COVID-19病毒通过破坏肠道细菌的正常混合,增加了其他感染的风险
一项新的研究发现,感染大流行病毒SARS-CoV-2可以减少患者肠道内细菌种类的数量,多样性的减少为危险微生物的繁殖创造了空间。
这项研究建立在广泛使用抗生素来对抗感染的认识之上致病的细菌近几十年来,通过消灭对现有药物最脆弱的物种,留下了更多对抗生素有耐药性的物种。此外,肠道细菌比例的中断此前曾与更严重的COVID-19有关。
然而,研究人员表示,到目前为止,尚不清楚冠状病毒是谁先出现的感染破坏了肠道微生物组或者已经虚弱的肠道使身体更容易受到病毒的攻击。新的研究似乎支持前一种解释。这项新的研究还揭示了耐抗生素物种可以逃逸到血液中,使患者面临更大的危及生命的继发感染的风险。
由纽约大学格Grossman医学院的研究人员领导的这项调查涉及了纽约市和康涅狄格州纽黑文于2020年因COVID-19住院的96名男性和女性。结果显示,大多数患者肠道微生物群落多样性较低,其中四分之一由单一类型的细菌主导。与此同时,已知包括耐抗生素物种在内的几种微生物的数量增加,这可能是由于大流行早期广泛使用抗生素造成的。
这些耐药细菌在20%的患者中,肠道中发现的细菌也被观察到迁移到血液中。该研究的作者指出,需要进一步的研究来揭示为什么这一组人继发感染的风险更高,而其他人仍然受到保护。
“我们的研究结果表明,冠状病毒感染直接干扰肠道微生物的健康平衡,在这一过程中进一步危及患者,”该研究的联合高级作者、微生物学家肯·卡德威尔博士说。Cadwell补充说:“现在我们已经发现了这种细菌失衡的来源,医生可以更好地识别那些最有二次血流感染风险的冠状病毒患者。”
这项新研究首次表明冠状病毒感染卡德威尔也是纽约大学朗格尼健康中心微生物和医学系的教授,他说,单独使用抗生素来治疗这种疾病,而不是像其他专家认为的那样,会损害肠道微生物群。他补充说,这项研究还提供了第一个证据,证明肠道中的同一种细菌也在进入患者的血液,导致危险的感染。
该报告于11月1日在线发表在该杂志上自然通讯.
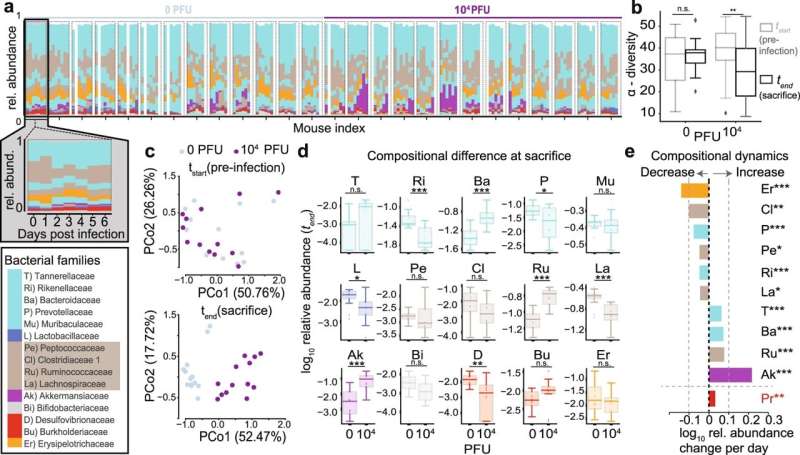
在这项调查中,研究人员首先用冠状病毒感染了几十只老鼠,并分析了它们粪便样本中细菌种类的构成。这一步使他们弄清了冠状病毒是否可以独立于住院和治疗直接破坏微生物组。
接下来,他们从纽约大学朗格尼医院和耶鲁大学医院收集了COVID-19患者的粪便样本和血液检测,以评估肠道微生物组成和继发感染的存在。如果任何一种细菌群占肠道细菌的大多数,那么它们就被认为是优势细菌。
“我们的研究结果强调了肠道微生物群和身体不同部位是如何影响人体健康的免疫系统是密切相关的,”该研究的资深作者Jonas Schluter博士说,他是纽约大学朗格尼分校微生物学系的助理教授,也是系统遗传学研究所的成员。“其中一个的感染可能会导致另一个的严重破坏。”
Schluter警告说,由于患者接受了不同种类的治疗,这项调查不能完全解释所有可能导致他们的微生物群被破坏并恶化疾病的因素。
Schluter说,研究团队下一步计划研究为什么某些微生物物种在COVID-19期间更有可能逃离肠道。研究人员说,他们还打算探索不同的微生物是如何相互作用的,这可能有助于这种迁移到血液中。