科学家揭示了大脑蛋白质在儿童运动障碍中的作用
北卡罗来纳大学医学院和北卡罗来纳大学埃谢尔曼药学院的科学家与伦敦玛丽女王大学的一个团队合作,阐明了一种遗传运动和神经退行性疾病的分子事件,称为arsacs - Charlevoix-Saguenay常染色体隐性痉挛性共济失调症,以发现第一例病例的两个魁北克山谷命名。
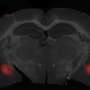
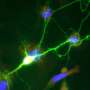
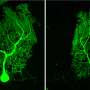
患有ARSACS的儿童通常在两岁时表现出行走困难,之后会出现一系列神经问题。小脑是大脑中协调运动和平衡的区域,在患有ARSACS的个体中,名为浦肯野细胞的神经元死亡。大多数患者在30到40岁时就必须坐轮椅,平均到55岁左右寿命就会缩短。
这种疾病是由一种名为SACS的基因突变和功能丧失引起的,这种基因编码一种叫做sacsin的非常大的蛋白质,由于其庞大的体积,一直难以直接研究。相对而言,人们对它的正常功能以及它的缺失如何导致疾病知之甚少。但一项发表在细胞的报道在美国,合作的研究人员对囊蛋白缺失时细胞内发生的情况进行了最全面的分析。
“我们试图采取一种公正的方法来了解细胞失去囊蛋白时发生了什么问题。我们的研究结果表明,ARSACS中浦肯野细胞的死亡可能是由于神经元连接和突触结构的变化,”该研究的共同高级作者Justin Wolter博士说,他是北卡罗来纳大学神经科学中心的博士后研究员。
该研究的另一位资深合著者是伦敦玛丽女王大学的分子细胞生物学教授Paul Chapple博士。
这项研究开始于查普尔实验室和北卡罗来纳大学教堂山分校的团队在彼此不知情的情况下开展工作。“这个项目是由北卡罗来纳大学埃舍尔曼药学院的Tammy Havener发起的,然后来自北卡罗来纳大学不同院系的三位博士后研究员——wen Aw, Katherine Hixson和我自己加入进来,”Wolter说。“当我们意识到查普尔实验室的丽莎·罗马诺用不同的方法做出了类似的发现时,我们都决定联合起来,共同前进。我认为这是一个很好的例子,说明了开放科学和合作如何为社区带来回报。”
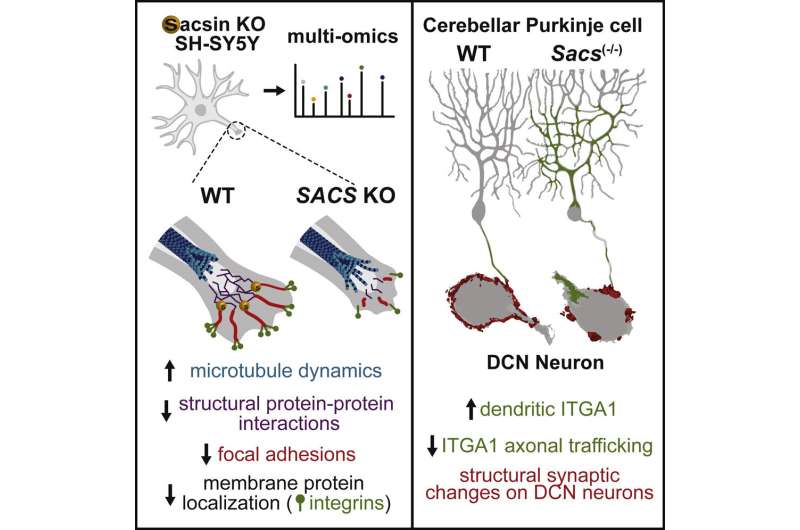
在这项研究中,研究人员在培养中使用了几种基于组学的技术人类细胞研究囊蛋白的丢失如何改变蛋白质水平和细胞组织。他们证实了之前研究中已经注意到的缺陷的存在,如纤维形成的异常聚集结构蛋白以及线粒体数量和动态的缺陷,这两者在许多神经退行性疾病中经常被观察到。
但他们也发现了许多以前没有发现的异常。其中包括一种叫做tau蛋白的蛋白质的过量和微管动态的改变,微管是受tau蛋白调控的细胞内运输轨迹。研究人员发现,这种运输变化的后果是许多蛋白质无法到达细胞内的适当位置。
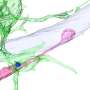
尤其受影响的是“突触粘附”蛋白,它帮助神经元形成和维持突触——神经元用来相互发送信号的连接。与这些观察结果一致的是,研究小组在ARSACS小鼠模型中发现了突触结构的变化。重要的是,这些变化发生在神经退行性变发生之前。
这些发现扩展了囊蛋白如何调节多种细胞过程的图景。他们还提出,浦肯野细胞(arsacs中受影响最大的神经元)可能因为缺乏与其他神经元的连接而死亡。研究人员将继续对大脑中的这些变化进行更深入的研究,以了解这种神经退行性疾病是否起源于大脑发育过程。
研究人员指出,尽管ARSACS可能只影响全球几千人,但这种研究可能有更广泛的影响。
“在ARSACS和其他大脑疾病之间似乎有很多重叠,”Chapple说。“例如,我们表明,在缺乏囊蛋白的细胞中,tau蛋白生物学被破坏,当然,tau蛋白异常也是阿尔茨海默病的一个众所周知的特征。所以我们认为,研究这种罕见的神经疾病可以为更常见的疾病提供见解。”
Wolter说:“要了解突触连通性受到影响的机制,以及它是否导致神经元死亡,还有很多工作要做。”“但是,如果是这样的话,它可能会为未来的治疗方法提供参考。”