创新技术揭示了瘢痕是如何在长冠状病毒和肺纤维化中发生的
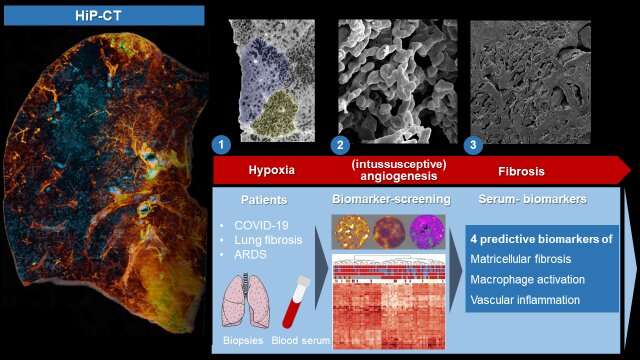
一个国际研究团队使用创新的血液生物标志物和x射线技术,揭示了长冠状病毒和肺纤维化中瘢痕是如何发生的。这项研究发表在eBioMedicine,有助于了解重症COVID-19的病理生理学,从而了解其治疗方法。
在大流行爆发两年多后,长COVID综合征或SARS-CoV-2感染长期后果的起源仍未完全了解。特别是长期的变化肺组织严重的COVID-19疾病对许多患者造成了重大限制。其中一些患者在covid后继续发展肺纤维化其特征是肺组织迅速形成瘢痕。
到目前为止,科学界还不了解这种疤痕的潜在机制,以及可以预测这一过程的特定血液标记物。
现在,由亚琛工业大学医院病理研究所、汉诺威医学院(MHH)、伍帕塔尔赫利奥斯大学医院和美因茨大学医学中心的医生和研究人员领导的一个国际研究小组,与伦敦大学学院(UCL)和欧洲同步加速器(ESRF)的科学家合作,发现了改变严重COVID-19肺部结缔组织的机制。
通过结合最新的成像和分子生物学技术,这个多学科团队发现了严重COVID-19患者肺部结缔组织发生改变的机制。他们已经证明了COVID-19如何改变肺部最细血管的结构,并在患者血液中发现了这种损伤的分子标记,最终可能有助于诊断和治疗这种疾病。
肺纤维化与COVID-19
术语“肺纤维化”包括各种不同的肺部疾病,其中持续的炎症导致肺支架的进行性瘢痕。虽然这些严重的疾病可以通过药物缓解,但它们仍然无法治愈,通常比许多癌症的死亡率更高。
对于许多患者来说,肺移植是唯一剩下的挽救生命的治疗方法。重症COVID-19患者的流行病学数据表明,约20%的住院患者出现了covid后肺纤维化,其程度和进展差异很大,只能通过常规临床影像学进行非常不准确的预测。
HiP-CT显示肺部损伤
为了首次详细揭示这一瘢痕过程中的微观组织变化,研究人员使用最新的3d成像技术——分层相位对比断层扫描(HiP-CT)——检查了严重病变的COVID-19的完整肺部,这种技术是在世界上最亮的同步加速器x射线源——法国的ESRF-European同步加速器上开发的。
然后,研究人员将通过HiP-CT获得的成像结果与临床结果进行了比较,并证明,与其他纤维化肺病和甲型流感相比,COVID-19的变化是由微凝块(医学上称为继发性小叶微缺血)和通过特定机制(称为肠套叠性血管生成)形成的新血管驱动的。
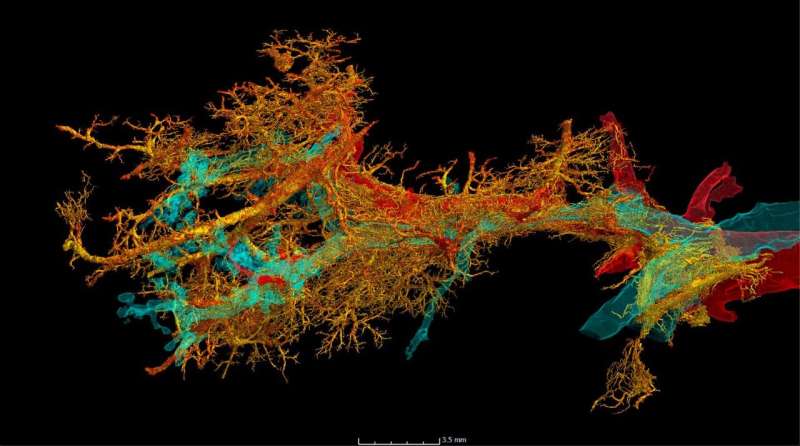
这种血管形成是COVID-19的典型特征,在COVID-19疾病的过程中显著增加。亚琛工业大学医院病理研究所的胸廓病理学家Danny Jonigk解释说:“由于目前的临床技术缺乏细节,这些分布不均的、在最细肺小叶水平上的明显变化无法通过临床成像检测到。”
“通过HiP-CT的新技术,我们第一次能够看到covid后纤维化的瘢痕过程是SARS-CoV-2病毒引起的全身性血管损伤的结果。”
来自美因茨和伍珀塔尔的第一作者Maximilian Ackermann指出:“这些结果表明,旨在预防微血管血栓形成和组织缺血的治疗(如早期补氧和抗凝)可能对严重COVID-19患者有益,并避免随后的纤维化重塑。”
HiP-CT是由UCL教授Peter Lee领导的UCL- esrf团队联合开发的一项技术。Lee解释说:“ESRF在同步加速器中是独一无二的,能够进行HiP-CT,这既是因为它的极亮源(EBS)升级,也是因为光束线BM18的许多独特品质。”
由Paul Tafforeau领导的ESRF团队使用HiP-CT首次表明,在严重的COVID- 19中,肺部损伤存在马赛克状模式。
伦敦大学学院的研究人员克莱尔·沃尔什(Claire Walsh)说:“了解一种疾病的模式在整个器官中是如何不同的,就像马赛克模式一样,有助于我们破译损害发生的机制。像HiP-CT这样的技术是真正的游戏规则改变者,它不仅揭示了组织损伤的真正细节,而且还揭示了它在整个器官中的分布情况,并将其与临床中看到的情况联系起来。”
研究小组还使用英国的同步加速器光源“钻石光源”来成像肺的一小部分,这表明肺组织血液供应的减少是由于供应肺的最细血管结构的变化。
用于早期纤维化检测的组织和血液生物标志物
该团队还发现了严重COVID-19和间质性肺部疾病的新组织标记物。汉诺威肺研究小组的Jan-Christopher Kamp说:“我们注意到炎症标志物和新血管形成标志物的显著增加,这是受影响患者临床恶化的原因。”“关键是分子数据与损伤的形态模式之间的相关性。”
对于国际研究团队来说,尤其重要的是,不仅要研究严重COVID-19疾病的组织标记物,还要确定早期纤维化重塑的血浆标记物,这些标记物可以作为COVID-19疾病严重程度和治疗反应的预测指标。
他们能够识别出三种“关键标记”,这些“关键标记”隐藏在大脑中肺组织,在单元格之间的空间。通过比较COVID-19和其他形式的肺纤维化(如特发性肺纤维化(IPF))患者的血液和组织生物标志物,研究小组可以将肺纤维化发展的早期形态和分子特征与肺纤维化中相关蛋白水平的升高联系起来血.
美因茨大学医学中心和哈佛医学院的Detlef Schuppan解释说:“这些‘预测血清生物标志物’使我们能够找到新的治疗方法,并尽早开始对受影响的患者进行治疗,当疤痕过程仍然可以通过药物治疗逆转时。”