对细胞“载体”的新分析推动了对ALS,阿尔茨海默氏症的更深入了解
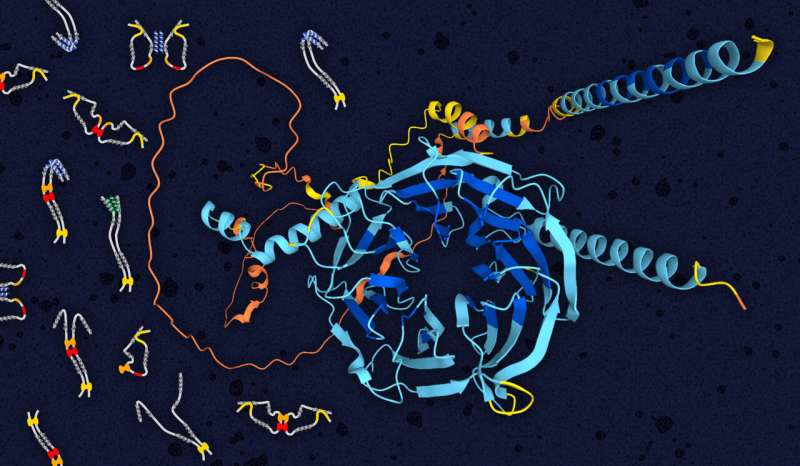
俄勒冈州立大学的科学家们通过使用一套生物物理技术来更多地了解一种运动蛋白,从而在更好地理解神经退行性疾病方面迈出了关键一步,这种运动蛋白的功能障碍与许多疾病有关。
的研究发表在杂志上eLife,代表着世界各地数百万受阿尔茨海默病等疾病影响的人在改善护理方面取得的重要进展,肌萎缩性侧索硬化症帕金森症和多发性硬化症。
神经退行性疾病发生在神经细胞在大脑中脊髓神经元会分解,功能异常,最终死亡。随着神经元的恶化,患者通常会经历一系列逐渐恶化的情况神经系统症状这可能会导致身体衰弱,在很多情况下甚至死亡。
根据哈佛神经发现中心的数据,美国有500万人患有阿尔茨海默病,100万人患有帕金森病。此外,还有40万名多发性硬化症患者和3万名ALS患者。1939年,棒球明星卢·格里克(Lou Gehrig)被诊断出患有ALS,这种疾病开始引起公众的注意。
神经退行性疾病主要发生在中老年,这意味着随着美国人口老龄化,发病率预计将上升。人口统计数据显示,如果没有新的干预措施,到2050年将有超过1200万美国人受到神经退行性疾病的影响。
俄勒冈州立大学理学院生物化学和生物物理系主任Elisar Barbar和俄勒冈州立大学遗传密码扩展中心GCE4All项目协调员Kayla Jara领导了对动力蛋白的深入研究,动力蛋白是细胞内两种运动蛋白之一;另一种是驱动蛋白。
马达蛋白是动物和真菌细胞用来将化学能转化为机械能的微小分子机器。它们是通过被称为细胞骨架的轨道网络穿越细胞的微型“车辆”,牵引细胞有效载荷并产生力量,以帮助许多重要的过程和功能。
“Dynein负责控制货物的运输细胞增殖以及损伤后和再生过程中神经系统的分化,”哈拉说。神经退行性疾病是由于产生动力蛋白马达部件的基因突变而引起的,并损害轴突的运输机制。
她说,神经细胞可以长得很长,严重依赖于运动蛋白,以确保细胞体和轴突尖端之间的物质运输。轴突是一条从细胞的主要部分延伸出来的电缆,用来传输信息电脉冲从一个神经元到另一个神经元。
“就像高速公路连接城镇和城市一样,在我们的细胞内有一系列被称为微管的道路马达蛋白芭芭尔说。“动力蛋白负责向一个方向运输货物,而大约40种驱动蛋白类型的蛋白质则负责向相反的方向运输货物。这表明,在组成动力蛋白的许多亚基蛋白之间存在复杂的调节方法。”
在这项研究中,Barbar和研究期间的博士生Jara与俄勒冈州立大学和刘易斯克拉克学院的科学家合作,仔细研究了其中一个亚基:中间链(IC),它作为其他亚基以及两种非动力蛋白(p150胶合蛋白和NudE蛋白)的粘结剂。
Barbar说:“这些结合作用都发生在IC的前半部分,许多结构技术都没有对其进行研究,因为它不会折叠成特定的结构。”“我们想要找出亚基的结合如何调节IC与p150glue和NudE的相互作用。由于研究非结构化的困难,这个问题一直没有得到回答蛋白质这种规模的复合体。但是p150glue和NudE结合在IC的相同区域,这些蛋白质参与不同的动力蛋白功能,所以必须有一种机制来选择两者。”
通过研究一种真菌——嗜热毛囊菌(chetomium thermoophilum)的蛋白质,科学家们了解到这种机制是什么:IC能够自我折叠并影响p150glue /NudE结合位点。由于对非结构蛋白质进行研究的挑战,许多生物物理技术被结合使用,Jara说,这导致了如何研究其他类似的蛋白质复合物的蓝图。
“动力蛋白是一种分子马达,负责运输错误折叠的蛋白质,使它们能够被分解,这意味着它至关重要地参与了蛋白质的出现和清除,而这些蛋白质是糖尿病的标志神经退行性疾病哈拉补充道。“特别是动力蛋白功能障碍是ALS和阿尔茨海默氏症等疾病的早期特征。有关动力蛋白结构及其工作原理的知识将有助于我们理解和治疗这些疾病。”
俄勒冈州立大学参与这项研究的其他研究人员有Patrick Reardon和Zhen Yu,以及本科生Prajna Woonnimani, Coban Brooks和Cat Vesely。刘易斯克拉克学院(Lewis & Clark College)的化学教授尼古拉斯·罗宁(Nikolaus Loening)也参与了研究。