长COVID:疲劳综合症的新证据的原因
长COVID综合征的诊断和治疗(LCS)仍然是非常困难的,只有小知识的因素导致伴随症状。联合代谢组研究人员设施维也纳大学和维也纳医科大学现在已经提出的新证据SARS-COV-2感染后会导致疲劳。
团队由化学家克里斯托弗要显示一个夸张的抗炎反应可能是负责LCS。这项研究已经发表在iScience。
今天数以百万计的人们遭受长COVID综合症(LCS),这大大影响了生活质量。然而,它是不容易诊断和治疗由于缺乏对潜在疾病机制的理解。联合代谢组研究人员设施(维也纳大学和维也纳医科大学)已经将注意力转向LCS利用大众spectrometry-based后基因分析技术。
这些方法的力量在于实际情况的全面的映射,即疾病的可追溯性过程发生在一个病人。克劳斯一起Schmetterer MedUni维也纳的实验医学和欧盟Gyongyosi,从维也纳MedUni´s医学系二世和维也纳总医院门诊长期COVID主管维也纳,病人群体选择和分析阐明LCS的分子基础。
典型的炎症标志物缺席
在病毒感染过程中,通常是一个非常强大的免疫系统的激活。但在几乎所有的长COVID病人研究,相应的标记如细胞因子、急性期蛋白质和类花生酸,这表明炎症,实际上是很难检测到。
急性炎症过程的“所有重要的潜在标记被以下水平的健康的捐赠者或者根本不检测LCS的病人,”研究报告的作者说,联合代谢物设施负责人克里斯托弗要。
令人惊讶的是,长时间的差异更加明显COVID患者相比无症状患者康复COVID疾病比健康对照组。“这一发现表明,确实有一些残留在无症状炎症反应检测到恢复的病人,而长COVID患者相反的发现,“要说。
尽管自身免疫之前怀疑长COVID的主要原因,目前没有证据表明伴随LCS患者的炎症过程。
相反,抗炎模式显示
与先前的预期相反,研究人员能够找到几个抗炎蛋白,脂质和代谢产物长COVID病人,这一方面可能导致最重要的LCS症状,另一方面指向另外极化的形成巨噬细胞的原因。
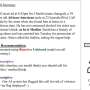
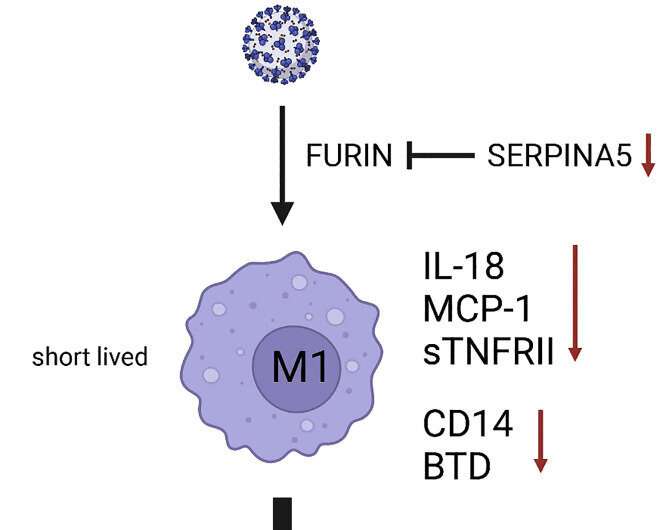
“抑制炎症的分子签名非常清晰可见,“要说。”例如,研究提供的证据表明,增加传染性的病毒可以通过解释缺乏急性期蛋白质(例如SERPINA5)。此外,研究人员能够表明,抗炎代谢物osmolytes牛磺酸和强烈上调hypaphorine LCS的病人。Hypaphorine自发诱导睡眠的动物,建议直接联系疲劳综合症”。
另外极化巨噬细胞主宰疾病模式
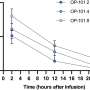
LCS患者的血浆分析允许病人的生理过程的深入见解。LCS的病人,一个积极参与的所谓或者极化巨噬细胞变得明显。这些细胞通常形成后各种感染和负责协调再生过程。分子概要文件中发现LCS的病人,包括蛋白质,脂类和代谢物,这些细胞的特征。
当然,这项研究并没有解决所有LCS-related问题。在与格哈德·Garhofer刚刚完成的一项研究中,从临床药理学的部门,联合代谢物设施调查的原因后动脉粥样硬化和心肌梗死的风险增加幸存的感染。
“LCS疾病的病理学是结晶越来越明显,这当然使一个全新的风险因素的评估和治疗选择,”该研究的作者说。研究人员相信,在不久的将来,他们将能够提供显著提高诊断LCS的选择,最重要的是,监控方法来评估治疗的效果。