CRISPR技术改善了模型中的亨廷顿舞蹈症症状
亨廷顿舞蹈症(HD)是一种神经系统疾病,会导致运动、协调和认知功能的进行性丧失。它是由一种叫做亨廷顿蛋白(HTT)的基因突变引起的。全世界有超过20万人患有这种基因疾病,美国约有3万人。超过25万的美国人有从受影响的父母那里遗传HD的风险。没有治愈方法。
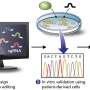
但在2022年12月12日发表的一项新研究中自然神经科学加州大学圣地亚哥分校医学院的研究人员和其他地方的同事描述了使用RNA靶向CRISPR/Cas13d技术开发一种新的治疗策略,专门消除导致HD的有毒RNA。
CRISPR是一种基因组编辑工具,允许科学家在基因组的特定位置添加、删除或改变遗传物质。它是基于细菌使用的自然免疫防御系统。然而,目前的策略存在在非预期位点脱靶编辑的风险,这可能导致永久性和可遗传的染色体插入或基因组改变。正因为如此,大量的努力集中在识别直接靶向RNA而不改变基因组的CRISPR系统上。
在HD的情况下,这种情况是由HTT基因中的重复和破坏性序列引起的。
“我们的细胞很难复制重复的DNA,这些复制错误会导致重复序列在每一代都变长,”资深研究作者、细胞遗传学教授Gene Yeo博士说分子医学加州大学圣地亚哥分校医学院
“在亨廷顿基因中,这些重复序列有时会增长到正常长度的许多倍,由此产生的重复扩增蛋白倾向于聚集并在大脑中被称为纹状体的部分形成有毒的团块,这对调节运动很重要。纹状体中功能性神经元的丧失最终导致HD症状。”
Yeo和他的团队与加州大学欧文分校和约翰霍普金斯大学的同事一起,研究了最近描述的RNA靶向CRISPR技术是否可以用于影响与HD相关的RNA (DNA指令和蛋白质生产之间的化学中间体)积累。
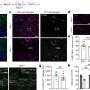
他们使用病毒载体将疗法传递到神经元培养物中,这些培养物是由干细胞他们发现,这种方法不仅靶向并破坏了突变的RNA分子,而且还清除了有毒的蛋白质积聚。他们还证明,其他人类基因的表达通常不会受到治疗的干扰。
Yeo实验室的研究员Kathryn Morelli博士说:“我们的目标是设计一种只针对导致HD的有毒RNA的治疗方法,并且可以保持人类基因组和转录组的其余部分完整。”“我们专门在HD患者的细胞系中筛选了我们的顶级治疗结构,以确保它。”
开发有效的HD疗法已被证明具有挑战性。例如,在2021年,两项有前景的基因疗法临床试验因结果令人失望而停止。这两种潜在药物都被吹捧为HD的游戏规则改变者。目前,虽然药物可以减轻一些症状,但没有任何治疗方法可以改变这种疾病的病程。
“亨廷顿舞蹈症社区被摧毁了临床试验失败了,主要是因为目标的特异性和毒性作用杨说。“但它们的终止只会重新激励科学界寻找替代策略。”
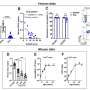
杨的实验室与约翰·霍普金斯大学医学博士、精神病学和行为科学教授段文珍合作,在小鼠身上进行临床前测试。段和共同第一作者吴谦博士发现,该疗法改善了HD小鼠模型的运动协调能力,减弱纹状体退化并降低了毒性蛋白水平。这种改善持续了至少8个月,没有不良反应,对其他RNA分子的脱靶效应也很小。