发现了儿童青光眼背后的新基因突变
由马萨诸塞州布里格姆总医院(massachusetts General Brigham)和波士顿儿童医院(Boston Children’s Hospital)的成员Mass Eye and Ear领导的一个国际科学家团队发现了一种新的基因突变,它可能是严重儿童青光眼病例的根本原因。青光眼是一种毁灭性的疾病,在家族中遗传,可以在3岁前夺走儿童的视力。
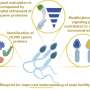
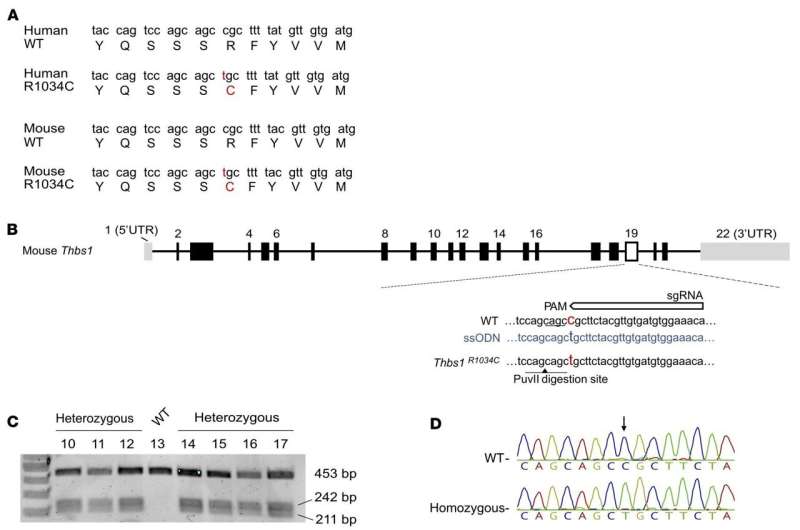
通过先进的基因组测序技术,研究人员在三个具有儿童青光眼病史的种族和地理不同的家庭中发现了血栓反应蛋白-1 (THBS1)基因的突变。研究人员随后在小鼠模型中证实了他们的发现,该小鼠模型具有基因突变,并继续出现青光眼症状,这是由一种以前未知的疾病机制引起的。
这项新发现发表在12月1日的《科学》杂志上临床研究杂志这项研究的作者说,这种方法可以改善对儿童青光眼的筛查,并更早、更有针对性地治疗,以防止携带这种突变基因的儿童视力下降。
“对于受儿童青光眼影响的家庭来说,这是一个非常令人兴奋的发现,”Janey L. Wiggs医学博士说,她是大众眼耳眼科临床研究副主任,也是哈佛医学院眼科临床研究副主席和Paul Austin Chandler眼科教授。
“有了这些新知识,我们可以提供基因检测,以确定家庭中可能有患病风险的儿童,并尽早开始疾病监测和常规治疗,以保护他们的视力。在未来,我们将寻求开发针对这种基因突变的新疗法。”
儿童失明的主要原因
儿童期青光眼或先天性青光眼是一种罕见但严重的疾病,早在出生时出现,晚至3岁。尽管青光眼很罕见,但它造成了全球5%的儿童失明病例。
青光眼对眼睛的视神经造成不可逆的损伤,通常是由于眼内压(眼压)的增加。在成年人中,这种损伤可能会随着时间的推移而发生,而没有症状,这就是为什么这种疾病通常被称为“视觉小偷”。
然而,患有儿童青光眼的儿童和婴儿出生时可能患有严重的疾病和视力丧失,或者由于眼压升高而在儿童时期失去视力。这种压力的增加不仅会损害视神经,还会影响儿童眼睛的其他结构,如角膜。患有儿童期青光眼的儿童通常在出生后的前3到6个月就需要手术,随后在整个童年期间还需要多次手术。
儿童期青光眼通常有很强的遗传成分,通常一个家庭的多个成员都患有这种疾病。据威格斯博士说,通过更好地了解相关基因,基因检测可以让受影响的家庭安心地了解他们的孩子是否有患这种疾病的风险。
揭示疾病的遗传基础
几十年来,研究人员已经转向遗传学,以更好地了解青光眼的原因。30年前,当威格斯博士第一次开始这方面的研究时,科学家们只能确定青光眼受影响的基因组区域。
由于基因组技术的进步,研究人员获得了检查青光眼患者和非青光眼患者的完整基因组成的能力,以确定其特异性基因突变在疾病中起作用威格斯博士在2021年领导的研究使用了3.4万多名青光眼成年人的数据集,确定了127个与这种疾病相关的基因。
为了更好地研究儿童青光眼的基因突变,威格斯博士和她的Mass Eye and Ear团队首先研究了来自一个欧洲-高加索血统的美国家庭的外显子组序列,该家庭曾是一个早期研究项目的一部分,并在血栓反应蛋白-1中发现了一个惊人的新变体,血栓反应蛋白-1是一种众所周知的蛋白质,参与了许多重要的生物过程,如新血管(血管新生)和组织的形成。
在没有童年青光眼的人群中没有发现这种突变基因,在大型人群基因数据库中也没有发现这种突变基因。被突变改变的氨基酸在进化上是保守的,表明在蛋白质功能中起着重要作用。这一发现促使威格斯博士与澳大利亚弗林德斯大学的同事联系,看看他们是否有血栓反应蛋白突变的儿童青光眼家族。
令人惊讶的是,他们发现两个家族在相同的氨基酸上发生了变化:一个是欧洲和印度混血,一个是来自非洲的苏丹家族。
“这一发现真正令人震惊的是,这些家庭都拥有这种基因变异,他们不可能有血缘关系,因为他们来自如此不同的背景,”威格斯博士说。“这意味着这种突变有一些非常重要的东西。”
为了进一步验证这一假设,研究人员与罗伯特·j·达马托(Robert J. D'Amato)医学博士合作,他是波士顿儿童医院血管生物学项目外科手术的Judah Folkman主席,也是哈佛医学院的眼科教授。达马托博士的团队开发了一种小鼠模型他们发现这只老鼠也有青光眼的特征。
“众所周知,血栓反应素-1是一种有效的血管生长或血管生成抑制剂,”达马托博士说,他研究血管生成已有30多年。“起初,我认为THBS1突变破坏了眼睛的血管形成,但我们的动物模型显示出正常的血管生成。我们意识到一定有另一种机制。”
具体来说,D'Amato的实验室表明,这种突变导致异常的血栓反应蛋白积聚在调节眼压的眼内引流结构中,这反过来又导致压力的积聚,损害视神经,导致视网膜神经节细胞的损失,从而导致视力下降。
这是研究人员首次发现导致儿童青光眼的这种疾病机制。
“这项工作突出了国际合作的力量,”该研究的合著者、弗林德斯大学和澳大利亚加文医学研究所的副教授欧文·m·希格斯医学博士、哲学博士说。ob欧宝直播nba“全球范围内的基因多样性令人难以置信,比较这些信息对于这样的发现变得越来越重要。”
为未来学习的家庭提供个性化的照顾
据研究人员称,这项新研究具有重要的临床意义。在全面之前还有更多的工作要做基因检测根据作者的说法,每一个被发现的基因都提供了另一个机会,能够通过筛查确定这些家族中的致病突变。
在治疗上,这种基因突变的知识可以导致早期的治疗与常规疗法。例如,如果婴儿出生时携带这种突变,他们的眼科保健专家可以更好地告知父母风险,并制定适当的疾病监测和治疗计划。
在儿童青光眼的根源上识别这种新机制和基因也可能导致针对异常蛋白质积累的新疗法。研究人员还旨在确定其他THBS1突变是否与成人发病的疾病有关,如原发性开角型青光眼,或者如果突变不那么明显,那么这种疾病的轻度形式。
研究人员还将继续寻找与儿童青光眼相关的新基因,希望有一天能开发出非常全面的筛查方法。
“威格斯博士是青光眼遗传学方面的国际专家,他孜孜不倦地研究基因对这些致盲疾病的影响。这些发现为研究儿童的成因提供了重要的见解青光眼并提供靶向治疗的前景,”医学博士琼·w·米勒说,她是马萨诸塞州总医院眼耳眼科主席,布莱根妇女医院首席眼科医生,哈佛医学院眼科主席和大卫·格伦登宁·科根眼科教授。
“这次合作有力地证明了从病床到工作台再到床边的转化研究的力量,它揭示了疾病的发病机制,并为患者开发了治疗方法。”