新冠肺炎患者“脑雾”的潜在新疗法
感染长冠状病毒的人有时被称为“长途跋涉者”,在急性病毒感染后,症状可能持续数周、数月甚至数年。虽然症状差异很大,但患者常见的抱怨是“脑雾”——这是一个俗语,指严重的、持续的认知缺陷,并伴有执行功能和工作记忆的持续损害。
长期工作的人可能会出现思维不清晰、注意力不集中、记忆力减退、难以同时处理多项任务等问题。脑雾会使人衰弱,但目前还没有针对这种情况的治疗方案。
虽然他们研究的患者数量太少,结果还不能确定,但耶鲁大学的研究人员利用他们对两种现有药物的丰富经验,发表了初步证据,证明这两种药物同时服用可以减轻甚至消除脑雾。
胍法辛由Amy Arnsten博士,Albert E. Kent神经科学教授和心理学教授的实验室开发,2009年被食品和药物管理局(FDA)批准用于治疗多动症,但临床医生也广泛使用它治疗其他前额皮质疾病,如创伤性脑损伤(TBI)和创伤后应激障碍(PTSD)。
现在,Arnsten与精神病学和神经病学助理教授Arman Fesharaki-Zadeh医学博士合作,他一直在用胍法辛和n -乙酰半胱氨酸(NAC)的组合治疗长时间COVID患者,n -乙酰半胱氨酸是一种抗氧化剂,也用于治疗TBI。
的联合治疗他们发现,这种方法成功地缓解了一小群患者的脑雾。虽然需要更大规模的安慰剂对照临床试验来证明这些药物是治疗covid -19后神经认知缺陷的真正治疗方法,但他们表示,如果医生希望开出这些药物,患者现在就可以获得它们。
Fesharaki-Zadeh说:“对于长时间的COVID脑雾,目前缺乏治疗方法,所以当我不断看到这种治疗在患者身上的好处时,我有一种传播这一信息的紧迫感。”“你不需要等待成为研究试验的一部分。你可以问问你的医生——这些药价格低廉,而且很容易买到。”因为它们是fda批准的,并且已经使用了多年,所以它们对患者的安全性是确定的。
研究人员发表了他们的案例研究在神经免疫学报告11月25日。
专注于大脑中具有独特属性的区域
执行功能、工作记忆和注意力调节是由大脑中最近进化出来的前额叶皮层执行的。这个区域的神经回路对炎症和压力“非常脆弱”,Arnsten说,他花了几十年时间研究认知背后的神经回路。
她说:“产生高级认知功能的回路有非常特殊的分子需求,因为它们必须在没有任何感官刺激的情况下产生神经活动——例如抽象的思想和记忆。”“神经元必须产生并维持自己的活动。”Arnsten说,炎症因子会干扰这些分子的需求,抑制电路的功能。因此,大脑雾。
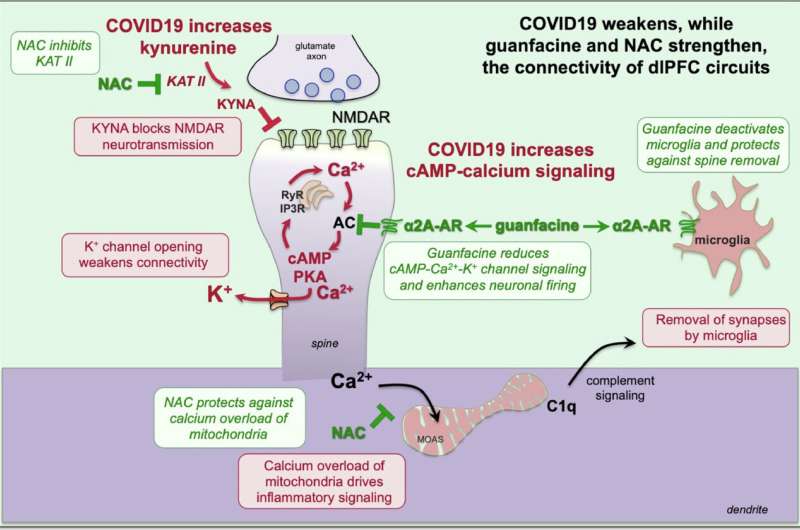
胍法辛是这项试验中测试的两种药物之一,旨在加强前额皮质的连接,防止炎症和压力。虽然最初是为了治疗多动症而开发的,但现在它被用于治疗与前额皮质功能障碍相关的其他疾病,研究表明,这种药物在恢复执行功能和记忆方面是有效的。NAC,第二种药物,是一种强大的抗氧化剂和抗炎剂,也可以用于治疗这一神经区域。
Fesharaki-Zadeh是一名临床神经科学家,对创伤性脑损伤和创伤后应激障碍有特殊兴趣,多年来他一直成功地用胍法辛和NAC联合治疗他的病人。在2020年6月遇到他的第一个长COVID患者后,他开始对使用这种疗法来治疗COVID后的脑雾感兴趣。
他说:“我有了从两个不同的角度来治疗的想法——用NAC改变促炎、促氧化途径,用胍法辛治疗影响执行功能的covid后神经认知后遗症。”“我们希望利用NAC和胍法辛之间的协同关系,利用多模型方法来解决这一问题。”
胍法辛和NAC缓解长时间COVID脑雾
面对他的第一个长时间的COVID病例,Fesharaki-Zadeh意识到他的病人面临的脑雾和脑震荡后病人的症状之间有重叠。因此,他开始使用NAC,它通常用于治疗脑震荡后的症状,并注意到在能量和记忆方面的部分好处。受到鼓舞后,他试着加入胍法辛,并看到了更大的改善。
从那时起,Fesharaki-Zadeh用这种疗法治疗了12名患有covid后脑雾的患者。他指导患者睡前服用1毫克胍法辛,如果耐受良好,一个月后将剂量增加到2毫克。患者还每天服用一次NAC,每次600mg。
8名患者报告了实质性的益处,包括记忆力、组织能力和多任务处理能力的改善。对于一些人来说,脑雾完全消失了,他们能够恢复正常的活动。两名患者无法进行随访,另外两名患者由于低血压和口干等副作用而停药。从那时起,研究人员将胍法辛的立即释放形式修改为延长释放形式,从而降低了副作用的风险。
队列中的一名患者是一名护士,她变得非常虚弱,不得不大幅减少工作时间。虽然她在治疗中得到了缓解,但由于头晕发作,她不得不短暂地停止治疗,她的认知缺陷又回来了。当她恢复治疗时,她的脑雾再次消散。从那以后,她再也没有头晕过。
“这不是一个安慰剂对照试验,但这样的轶事让人更加相信,缓解真的是由于药物,而不是安慰剂效应,”Arnsten说。
Fesharaki-Zadeh说:“她需要在最需要她的时候大幅减少工作时间。”“治疗她的病情不仅帮助了她,也帮助了我们所有人。”
为长期感染新冠病毒的患者和其他人带来希望
当一个又一个病人开始报告病情缓解时,费沙拉基-扎德变得兴奋起来。对于他的大多数患者来说,这是第一次成功地缓解他们的脑雾。
他说:“我被这些年轻人所震惊,他们被这种持续存在的疾病所摧毁。”“作为一名医生,一开始我感到无能为力。我们感到迫切需要发布这一病例报告,以便更多的患者得到治疗。”
研究人员希望他们的案例研究能够为安慰剂对照研究提供资金支持临床试验涉及接受这种治疗的更大的患者队列。但是那些被这些症状弄得虚弱不堪的长途跋涉者现在需要治疗。幸运的是,研究人员说,他们可以向医生索要胍法辛的处方,而NAC在柜台上就能买到。
“如果病人的医生能阅读我们的论文,我们希望他们现在就能得到帮助,”Arnsten说。
研究人员还希望这种疗法对其他患者也有帮助。长冠并不是唯一引起的病毒后综合征脑雾-例如,患有后莱姆病和肌痛性脑脊髓炎/慢性疲劳综合征(ME/CFS)的患者也会出现使人衰弱的认知缺陷。
事实上,Fesharaki-Zadeh在治疗一名莱姆病后患者时已经看到了有希望的结果。此外,治疗可能对其他炎症情况有益。他还在一位患有认知和记忆缺陷的多发性硬化症(MS)患者身上发现了认知方面的好处。
“我非常感谢我与Amy Arnsten的合作,以及我对她的理解创伤性脑损伤可能会有帮助,”Fesharaki-Zadeh说。“我们的成功是在正确的地点和时间拥有正确的知识,同时与正确的人合作的结合。”