重新思考癌细胞是如何逃避靶向治疗的
胶质母细胞瘤(GBMs)是一种无法治愈的脑肿瘤,平均预后约为一年半。他们对治疗有很强的抵抗力,并藐视所有精确治疗的尝试。
在他们12月20日发表的研究中自然癌症第一作者王林博士和资深作者Aaron Diaz博士发现,与遗传进化相反,表型切换可能是解释迄今为止精确治疗失败的逃避机制。他们发现,在标准治疗后,作为应激反应,一些细胞会转变为间充质、抗辐射表型(状态)
加州大学旧金山分校威尔神经科学研究所神经外科副教授迪亚兹说:“我们询问是否有另一种机制可以解释治疗耐药性。”“我们的研究得出的结论是,与基因进化不同,存在一种表型可塑性或转变,使这些细胞能够逃避治疗。”
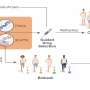
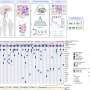
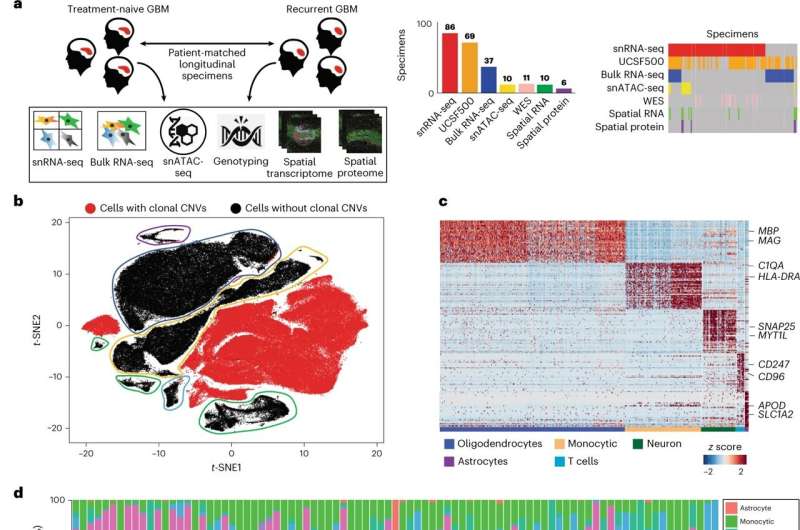
为了确定是什么驱动了对标准治疗的耐药性,以及复发性疾病的细胞来源,UCSF的研究人员使用单核RNA、开放染色质、空间分析来分析86个原发性复发、患者匹配、配对的GBM标本。这个前所未有的队列代表了UCSF几十年的生物银行。
通过获取30年的GBM数据,科学家们能够提出新的细胞内禀和细胞外禀靶点,以及治疗中的GBM单细胞多组学图谱。这是研究人员第一次能够在复发性GBM的肿瘤解剖利基中全面绘制细胞内信号,并确定新的细胞外源性治疗靶点
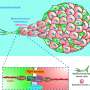
86个标本包含细胞肿瘤和邻近的手术边缘的非恶性组织。这个独特的队列使Diaz和他的团队能够分析恶性和非恶性胶质细胞之间的通信。他们发现手术边缘的细胞充当了复发的壁龛,在那里,非恶性胶质细胞发出了促进生长的信号,影响了肿瘤的生长肿瘤细胞再生。这些旁分泌(细胞外源性)信号刺激激活蛋白(AP1)通路,导致间充质转化、治疗耐药和肿瘤复发。
治疗后,这些间充质转化在肿瘤样本中很明显,并且循环次数增加间充质细胞.来自肿瘤微环境的促生长信号,以及细胞对放射治疗的内在反应,推动了间充质细胞的转移应激反应AP1介导的通路。
研究人员能够结合两种技术来实现旁分泌信号图-冷冻组织标本的单核rna测序和福尔马林固定标本的空间转录组学分析。从每个肿瘤活检后,他们进行了单核rna测序,测量转录组范围内的基因表达单个细胞,一次数千个细胞。
他们比较了信号受体的表达与其已知配体的表达,在不同的测序细胞群之间。然后他们进行了验证细胞利用空间转录组学,这些种群在原位物理相互作用并发出信号。
“这是第一次在胶质瘤中进行这种规模的单细胞纵向研究,”迪亚兹说。这也是一项只有在UCSF才能完成的研究,因为它代表了数十年来对外科标本的仔细生物银行。由于所有样本都来自UCSF,我们知道治疗历史是相同的,因为每个患者只接受标准护理治疗。正是这个队列的规模和治疗的一致性,使我们能够看到过去患者对疾病潜在生物学的特定影响。”