副作用的风险从癌症免疫疗法与遗传有关

即使他们已经彻底改变了癌症治疗,药物被称为免疫抑制剂检查站可以产生一系列的不良,免疫相关的副作用。在一项新的研究中,丹娜-法伯癌症研究所的科学家们发现,第一次,遗传基因变异,这些并发症的高危患者。
今天在网上报道了这一发现,《华尔街日报》自然医学,是由一个数学模型,允许调查人员使一个非凡的分析的飞跃:使用关于癌症相关基因突变在肿瘤组织的数据,研究人员能够推断出病人的基因遗传的特性。他们发现特定患者生殖系variants-common遗传基因改变的可能性增加发展中autoimmune-like副作用检查点抑制剂治疗。
通过识别这些患者治疗前模型和tumor-profiling技术已经在许多美国癌症centers-doctors可以修改疗法副作用降到最低,该研究的作者说。
“免疫抑制剂检查站在多种癌症类型是非常有效的,但病人常常经历的几种毒性,其中一些可能会很严重,”说,文章的第二作者亚历山大Gusev博士,dana - farber,麻省理工和哈佛大学,布莱根妇女医院。
“努力识别高危病人毒性也主要集中在肿瘤组织的基因方面。我们假设在这个研究病人的生殖系遗传影响开发这些毒性的风险。”
大约20%的患者检查点抑制剂开发温和严重的副作用——图一致的所有癌症药物的批准。与相关的副作用反映自身免疫性疾病:皮肤问题,疲劳、关节痛、反复发热、结肠炎、,在严重的情况下,心肌炎、心肌炎症。
这些症状是由于过于放肆的免疫系统的攻击。抑制剂检查站工作通过降低免疫系统攻击的障碍癌症细胞,而是因为正常细胞部署一些相同的障碍,他们也可能会受到批评。
看看病人的生殖系细胞内遗传物质dna线索对此类事件的敏感性,研究人员进行了一次全基因组关联研究(GWAS)的1715名患者接受治疗与检查点抑制剂在12癌症类型。gwas帆布基因组部分是否因人而异往往是与一个特定的疾病。
通常,这涉及到技术,读取每个字母的DNA,以病人的正常细胞(通常,血液细胞)。在新的研究中,然而,卡西和他的同事们设计了一个方法与手头的数据已经从GWAS研究基因组分析病人的肿瘤组织。
作为配置文件的一部分程序丹纳-法伯,研究中的1715名患者的肿瘤组织进行扫描了约500个基因的突变与癌症有关。虽然这帮助确定在这些肿瘤遗传缺陷,它没有排气基因组为每一个收集的数据。卡了数学模型使用原始数据概要文件生成读数的病人——以及识别任何变化。
“我们从500个基因靶向的肿瘤,现在,常见的全基因组变化在这组患者中,“卡西讲话。
与基因组数据,研究人员分析了患者的医疗记录,看看那些经验丰富的中度到重度的检查点抑制剂的副作用进行任何常见的基因变异。他们找到了一个连接到三个这样的变化,其中最突出的是基因IL7附近。然后他们确认这些发现在196年,一群2275年在马萨诸塞州综合医院和患者参加临床试验的患者的抑制剂atezolizumab检查站。
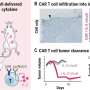
“在我们最初的患者群,我们发现检查点inhibitor-related毒性是三倍的速度在患者基因组改变IL7附近”研究文章的第二作者托尼Choueiri说,丹娜-法伯的医学博士。“在病人的其他两组,毒性率高出五次IL7组。”
“众所周知IL7基因有助于稳定淋巴细胞(白细胞帮助对抗疾病),”马修·弗里德曼指出,医学博士,丹娜-法伯,也是一个研究的文章的第二作者。研究人员发现患者窝藏IL7生殖系变异检查点期间及之后有更大的淋巴细胞稳定剂治疗,和这个稳定与不良事件的风险更高,提高生存。
稳定的生物学意义,有力的淋巴细胞可能是负责autoimmune-like副作用和激烈攻击肿瘤,延长病人的生存,研究人员说。
这项研究提供了第一个证据表明遗传变异能够标记增加易感性相关的几种副作用检查点抑制剂治疗。这一发现可能最终帮助肿瘤学家进一步个性化治疗的病人:这些发现可能经历严酷的副作用可能建议那么激烈或短疗程的治疗,而在低毒性的风险可能受益于更高的剂量或更积极的治疗,该研究的作者说。