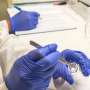
热稳定微针疫苗技术策略
生物医学工程系(康涅狄格大学牙科医学院、医学学院和工程学院的一个共享部门)的研究人员解锁了一种新策略,使用糖分子来热稳定现有的微针疫苗技术,消除了冷链存储的需要。
工程学院机械工程系和生物医学工程系的副教授Thanh Duc Nguyen在最近一期的《生物医学工程》杂志上报告了这一新进展先进材料技术.
这项工作由陈庆博士(Nguyen的前康涅狄格大学博士生,目前在麻省理工学院)和泰勒·加维特博士(前康涅狄格大学博士生,目前在杜克大学)领导。加维特是康涅狄格大学农业、卫生和自然资源学院病理生物学和兽医科学系史蒂文·什切帕内克副教授的学生。
一般来说,预防疫苗传染病如COVID-19需要多次痛苦、昂贵和不方便的注射,包括一次主要注射和几次加强注射。康涅狄格大学研究人员的技术创造了一种自我管理的微针贴片,可以自我管理,只需要一次注射到皮肤-类似于尼古丁贴片-来执行疫苗的释放配置,模拟多次注射的效果。
然而,冷链储存的必要性是另一个物流障碍疫苗分布。
Nguyen说:“虽然可以快速设计和制造mRNA疫苗来应对COVID-19等大流行性病毒,但全球疫苗接种运动需要一种更传统的基于蛋白质的疫苗,这样就可以在世界各地已经建成的疫苗生产设施中进行大规模生产,并在全球范围内分发。”
“不幸的是,这些基于蛋白质的疫苗,类似于mRNA,在高温下非常不稳定,需要在低温下储存低温在昂贵的冰柜中,温度低于80°C。这成为疫苗运输和分发的一个重大后勤负担,因为世界上许多发展中国家和农村/偏远地区无法负担这种冷链储存条件。”
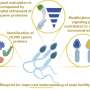
研究人员发现糖分子海藻糖和蔗糖是帮助稳定重组SARS-CoV-2 S1-RBD蛋白抗原(从COVID-19病毒外壳投射的蛋白质)的两种关键成分。在以水为基础的环境中,蛋白质的3D结构在高温下会发生错误折叠——类似于煮鸡蛋时蛋白变硬的过程。这会破坏疫苗的抗原蛋白。干燥的蛋白质会更稳定,但不小心去除水分也会破坏蛋白质的结构。
研究人员之所以选择海藻糖和蔗糖,是因为它们能够作为水的替代品,并与蛋白质形成氢键,以防止蛋白质错误折叠。高粘性的糖环境也有助于最大限度地减少蛋白质的流动性和暴露在环境中,防止进一步的不稳定。
在这项研究中,研究人员将海藻糖-蔗糖溶液以几种不同的比例与重组SARS-CoV-2 S1-RBD蛋白混合,并将混合物真空干燥过夜。样本暴露在高温下进行1小时的短期稳定性筛查,然后进行2、4、8、12和16周的长期稳定体温筛查。
研究人员证实,通过这种配方,他们的疫苗技术可以在极端温度下储存至少一个小时,在体温下储存至少四个月。这是首次报道的用海藻糖和蔗糖配方稳定特定重组SARS-CoV-2 S1-RBD蛋白的努力。
“用稳定的重组SARS-CoV-2 S1-RBD加载微针贴片蛋白质在大鼠中诱导了针对不同毒株SARS-CoV-2病毒的结合和功能性中和抗体反应,从而证明了该技术成为传统疫苗接种模式的可行的无针替代方案的潜力。这可以通过避免重复注射、训练有素的医务人员和疫苗储存的冷链设施,彻底改变全世界的疫苗接种过程,”Tran说。