研究发现晚期前列腺癌的潜在治疗方法
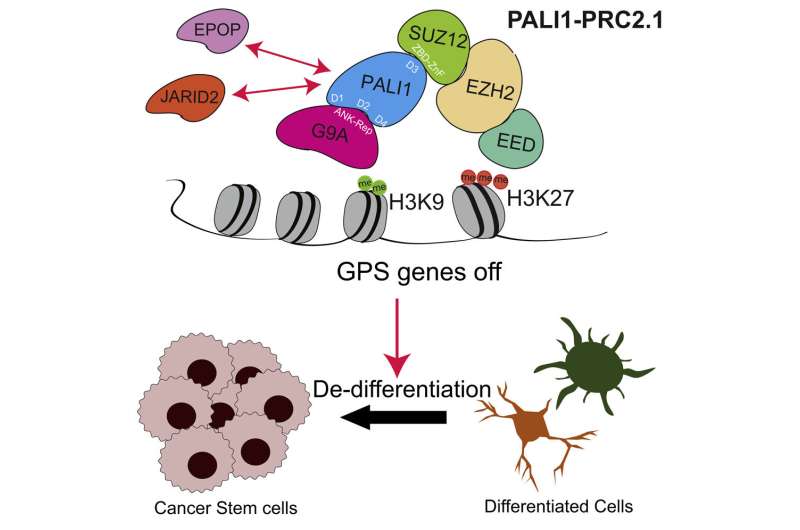
美国西北大学的一项研究发现,晚期前列腺肿瘤中PALI1的升高介导了两种主要表观遗传沉默机制之间的相互作用,这表明双重表观遗传抑制可能是一种有效的治疗策略分子细胞.
“我们发现PALI1在桥梁和利用两种主要的表观遗传沉默机制中的关键作用基因镇压和肿瘤促进强烈主张组合使用各自的药物抑制剂,”血液和肿瘤学部医学教授、该研究的高级作者金丹·余博士说。
许多癌症的一个显著特征是由去分化引起的不受控制的生长,当分化的细胞忘记自己的身份并重新获得谱系可塑性时,就会发生去分化。在之前的工作中,PALI1被确定为Polycomb抑制性复合体2 (PRC2)的附属蛋白,PRC2通过沉默必要的基因维持干细胞的多能性细胞分化.
PRC2的核心亚基是最强烈上调的基因之一晚期前列腺癌.虽然目前已知有几个PRC2基因在晚期前列腺癌中上调,但新发现的PRC2辅助蛋白PALI1的作用尚未完全了解。
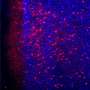
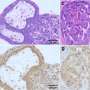
在目前的研究中,研究人员使用免疫共沉淀和全基因组定位分析来确定转移性前列腺癌细胞中新的蛋白质相互作用和细胞内蛋白质结合机制,并使用异种移植模型来研究晚期前列腺癌肿瘤的基因功能。
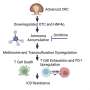
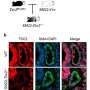
他们不仅发现PALI1被上调,而且该蛋白还与JARID2蛋白竞争与PRC2的结合,并直接与G9A相互作用蛋白质驱动细胞增殖和入侵。
值得注意的是,PALI1连接了PRC2和G9A蛋白之间独特的相互作用,两者都在G9A-PALI1- suz12 (GPS)一组基因的表观遗传沉默中发挥作用,这些基因参与细胞分化并在肿瘤发生过程中被抑制。
“因此,PALI1强烈抑制分化基因,诱导癌细胞干性并促进肿瘤的生长Yu说,他也是 生物化学和分子遗传学的教授,也是西北大学Robert H. Lurie综合癌症中心的成员。
据Yu说,GPS基因的丢失与不良的临床结果有关,使用互补抑制剂靶向PRC2和G9A可能具有治疗潜力。
Yu说:“幸运的是,GPS可以通过使用各自的抑制剂同时靶向PRC2和G9A来拯救,这种治疗方法可能有益于大量晚期前列腺癌患者。”
展望未来,Yu说她的团队旨在描述PALI1的其他关键功能前列腺癌她说,在癌症和其他类型的癌症中,研究结果可以推动从临床到临床的翻译。
“我们的研究是第一次深入研究PALI1在癌症中的作用。我们也是第一批在人类环境中研究PALI1的人,因为关于PALI1的有限研究主要是在小鼠身上胚胎干细胞于说。“我们开发了针对人类PALI1的试剂基因这些蛋白质将有助于研究PALI1在各种人类疾病中的作用。”