2023年1月30日功能
SARS-CoV-2的进化史导致一种通用疫苗已经在动物模型中进行了测试
通过从SARS-CoV-2本身的进化史中获得灵感,中国科学家研制出了一种新疫苗,至少在动物模型中,它可以提供对欧米克隆及其一系列亚变种的保护。
尽管早期的SARS-CoV-2疫苗和增强剂非常成功,但病毒进化和免疫逃避的出现使后续疫苗的生产更加困难。疫苗学家一直在问:我们如何跟上快速进化的病原体?冠状病毒似乎总是领先几步,尤其是现在,随着欧微米子变体继续进化出更敏锐的免疫逃脱能力。
科学家们说,尽管信使rna疫苗在过去两年中已经成为无价的工具,但还需要更多的疫苗方法。
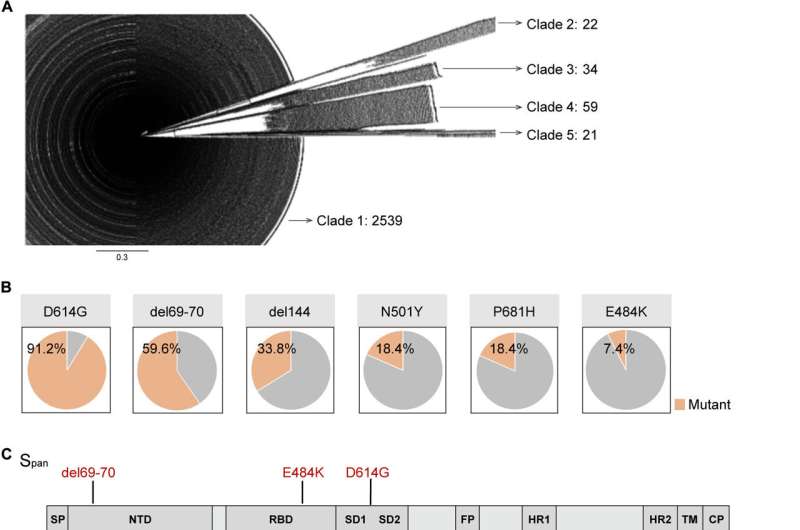
事实证明,病毒传播峰值蛋白质在最近的SARS-CoV-2变种中保持高度保守的区域。这些保守的区域是名副其实的进化数据目录,用于制造下一代疫苗。的斯派克蛋白质是病毒的末端,它与人类ACE-2受体结合,引发感染。
为了解决免疫逃逸的关键问题,并开始开发新疫苗的艰巨任务,中国武汉大学病毒学国家重点实验室的赵永亮博士和同事们希望在未来用一种新的疫苗来削弱亚变异的影响。
他们已经在实验室小鼠身上测试的实验性疫苗是基于刺突蛋白的保守区域,这意味着疫苗与刺突中很少突变的部分紧密相连。
武汉的研究小组对他们的研究悄悄表达了乐观态度,他们希望这将成为未来疫苗的一个模型,一种泛保护性免疫——一种预防现有变异和未来可能出现的威胁的通用疫苗。目前疫苗的一个关键问题是,尽管它们可以预防严重的疾病在美国,这种病毒的新版本,比如omicron越来越多的亚变种,可以逃过免疫系统的防御。
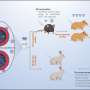
赵和来自武汉几家研究机构的合作团队通过询问SARS-CoV-2的进化轨迹开始了新疫苗的开发。作为研究的关键部分,他们分析了1100多万条SARS-CoV-2序列,以及54种SARS-CoV-2假病毒和变种的传染性和免疫逃逸能力。
实验表明,病毒突刺蛋白并不是随机进化的,而是朝着高传染性与低免疫逃逸配对或低传染性与高免疫逃逸配对的方向进化。
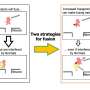
在此基础上,研究小组设计了一种以名为Span的新工程抗原为中心的疫苗。名字中的字母“S”代表“刺突”,就像病毒刺突蛋白一样,而“pan”来自希腊语,意思是“所有”,指的是针对所有刺突蛋白的疫苗。从另一个角度来看pan这个词,将它与希腊单词demos的一个版本结合起来,demos的意思是人,你会得到“pandemic”,一种影响所有人的疾病。
赵和他的同事在杂志上写道,开发研究性Span疫苗并不容易科学转化医学.“新冠病毒继续积累突变以逃避免疫,导致接种疫苗后出现突破性感染,”Span疫苗研究的主要作者赵说。
“研究人员如何在设计下一代疫苗时提前预测病毒的进化轨迹,这需要调查,”赵继续说道。“在这里,我们对11,650,487个SARS-CoV-2序列进行了全面研究,结果显示,SARS-CoV-2刺突蛋白不是随机进化的,而是朝着高传染性+低免疫耐药性或低传染性+高免疫耐药性的方向进化。”
斯潘抗原包含氨基酸残基迄今为止,在所有主要变种中都发现了很高的频率,这使它能够抵御进化上的谱系分歧。到目前为止,当斯潘疫苗在实验室的动物模型上接种时,已经促进了针对各种SARS-CoV-2变体的中和抗体。
赵和他的合作者测试了创新的Span疫苗和一种由缺乏Span进化嫁妆的野生型刺突蛋白制成的疫苗。研究人员发现,接种Span疫苗后的免疫反应比基于野生型spike的疫苗更有效蛋白质.动物模型(在这种情况下,小鼠)在注射Span疫苗时完全不受omicron变异的影响。
赵教授说,武汉的研究小组需要对疫苗对更多最近出现的欧微米子变异的有效性进行额外的测试,特别是最近几个月出现的那些。研究人员还警告说,Span接种需要在动物模型上进行更多的测试,而不是在实验室小鼠上进行,以更好地了解疫苗的优缺点。“在翻译之前,包括更多的动物模型是至关重要的疫苗到(人类)临床试验,”赵总结道。
更多信息:用SARS-CoV-2 S蛋白进化引导的抗原S pan接种疫苗,可在小鼠体内抵御病毒变异的挑战,科学转化医学(2023)。DOI: 10.1126 / scitranslmed.abo3332
©2023科学欧宝app网彩X网络