白血病遗传基础的新见解
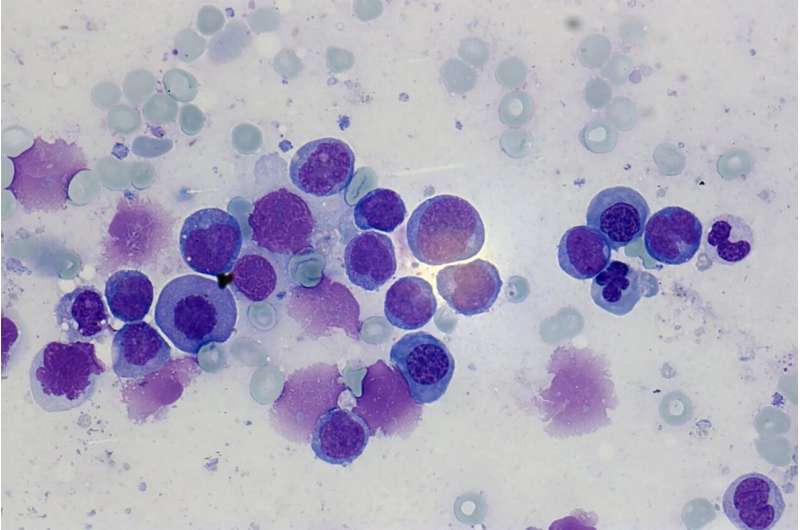
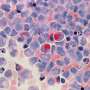
急性髓系白血病(Acute myeloid leukemia, AML)是由红细胞、血小板和部分白细胞的未成熟前体引起的一种恶性造血系统疾病。在健康人体内,血细胞的增殖和更新受到严格的调控,但在急性髓系白血病中,这一过程失去了控制:所谓的髓系细胞的早期前体退化和增殖不受控制。
这些前体在骨髓中迅速扩散,阻止健康血液成分的形成,最终损害血液系统的重要功能。这种疾病的病因尚未得到充分研究,可能与各种基因变化有关,其中一些是在一生中获得的。
虽然AML是成人急性白血病中最常见的形式,约占80%,但它是一种罕见疾病,每年每10万人中约有3例新发病例。随着年龄的增长,患者的预后恶化,复发和治疗耐药性的风险增加。
来自基尔大学医学院和大学医学中心石勒苏益格-荷尔斯泰因州(UKSH)基尔校区的内科II、血液学和肿瘤学诊所的一个研究小组现在调查了一种疾病基因突变这也从脑肿瘤研究中得知,可能与随着年龄增长的进展和预后恶化有关。AML患者的大量基因组数据显示,这种所谓的IDH1突变在65岁以后发生的频率明显更高。
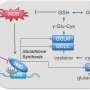
原则上,这种突变与某种代谢蛋白的形成有关细胞分化从而使血细胞成熟。然而,研究人员现在已经能够描述这种形式的白血病的一种以前未知的机制,这种机制会导致DNA三维结构的破坏,从而导致某种促癌基因的激活。
来自基尔肿瘤网络(KON)和石勒苏益格-荷尔斯泰因大学癌症中心(UCCSH)的Claudia Baldus教授领导的科学家,以及合作机构,最近在《柳叶刀》杂志上发表了他们的研究结果白血病.
被破坏的3D DNA结构
在癌症中,许多不同的因素经常相互作用,导致疾病的发展。因此,科学家们正在寻找能够解释某些与癌症相关的激活的基因模式基因.从以前的研究中已经知道,所谓的IDH1突变与DNA甲基化的全基因组增加有关。
甲基化是一种DNA的化学变化,在健康人体内,它能特异性地开启或关闭某些基因,从而调节由这些基因形成的蛋白质的数量。如果DNA甲基化增加,这被称为超甲基化。如果这影响了负责分化成成熟血细胞的基因,它们就不能被正确激活,受影响的细胞就会继续分裂而不是分化。其结果是疾病恶化得更快。
此外,脑肿瘤研究的新结果现在提供了证据,证明高甲基化也会导致细胞核中DNA空间结构的改变,这可能导致具有IDH1突变的脑肿瘤患者中癌症相关基因的激活。
在新的研究工作中,基尔大学的科学家们调查了DNA的这些3D变化是否也在白血病的发展中发挥作用。
“我们发现,高甲基化不仅影响已知的分化基因,还可能发生在所谓的CTCF结合蛋白的结合位点。通常情况下,这些结合位点决定了DNA在空间上的排列方式,相邻的结合蛋白切断了DNA环,然后将某些基因与其他遗传信息隔离开来,”Sophie Steinhäuser博士说,她是急性白血病功能基因组学组的研究助理。
“然而,由于这些结合位点的甲基化错误,这些环不能正常形成,以前分离的基因现在可以与外部的激活元件接触并被激活,”Steinhäuser继续说道。
在携带IDH1突变的AML患者中,这会导致PDGFRA基因的上调,该基因属于酪氨酸激酶家族。这些酶是细胞受体系统的一部分,传递细胞生长的信号,这在癌症的背景下也是相关的。在AML的背景下,PDGFRA的上调确实与IDH1突变患者的预后较差有关。
为了建立PDGRFA基因激活和DNA结构破坏之间的联系,研究人员使用了所谓的细胞模型。他们使用基因组编辑产生了具有IDH1突变的血癌细胞,并观察到癌症相关基因在这些人造细胞中也大量存在。
Steinhäuser说:“然后,我们检查了细胞模型中DNA的甲基化,并能够证明,在突变细胞中,包围PDGFRA基因的结合位点之一确实被甲基化了,因此基因的分离被破坏了。”研究人员认为,这证实了这种机制在之前未知的IDH1突变的促癌潜力中起着作用。
伴有IDH1突变的AML的潜在治疗方法
通过识别这一新颖的过程,研究人员发现了一种可能用于改善治疗方案的方法。原则上,酪氨酸激酶可以被抑制以抑制不受控制的细胞生长,这一选择已经在其他癌症中使用。“在各种实验中,我们已经测试了一种已经批准的药物,用于抑制具有IDH1突变的白血病细胞的酪氨酸激酶,”医学院急性白血病功能基因组学工作组负责人Baldus解释说。
“无论是在人工细胞模型还是在实验动物体内研究中,我们都观察到这种药物可以减少白血病细胞在血液,骨髓和脾脏。这是一种潜在的有前途的方法,将来可以考虑用于与IDH1突变相关的AML的更具体的治疗,”鲍德斯说,他是内科学II诊所主任和石勒苏益格-荷尔斯泰因大学癌症中心(UCCSH)的董事会成员。
在未来的研究中,科学家们希望进一步研究这些方法,以便为这类随着年龄增长尤其危险的AML患者开发更有针对性的治疗方案。
更多信息:Sophie Steinhäuser等人,异柠檬酸脱氢酶1突变通过PDGFRA激活驱动急性髓系白血病(AML)中绝缘体破坏的白血病发生,白血病(2022)。DOI: 10.1038 / s41375 - 022 - 01751 - 6