KRAS突变可促进肺癌固有免疫监测的肿瘤逃避
KRAS是人类癌症中最常激活的致癌基因之一。虽然KRAS突变在肿瘤发生和肿瘤维持中的作用已被广泛研究,但KRAS与肿瘤免疫微环境之间的关系尚不完全清楚。在这项研究中,研究人员确定了KRAS在驱动肿瘤逃避先天免疫监测中的新作用。
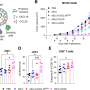
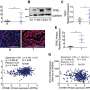
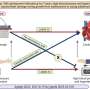
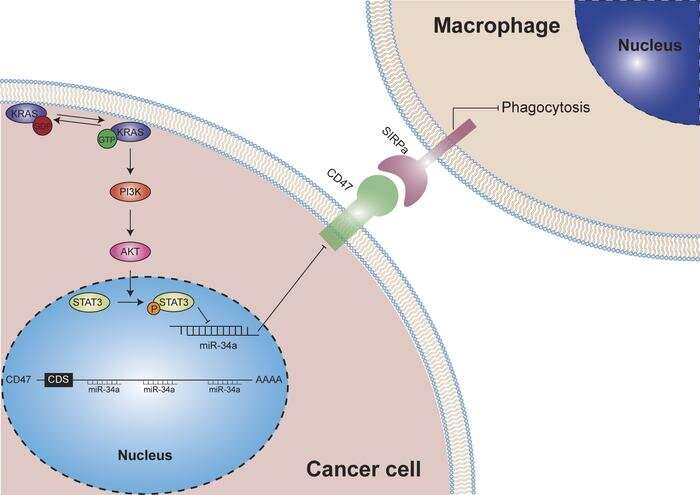
在肺腺癌患者样本和KRAS驱动的肺癌遗传小鼠模型中,突变的KRAS激活CD47的表达,CD47是一种抗吞噬细胞信号癌症细胞,导致巨噬细胞对癌细胞的吞噬能力下降。在机制上,突变KRAS激活PI3K-STAT3信号通路,抑制miR-34a表达,缓解miR-34a在CD47上的转录后抑制。
在三个独立的肺癌患者队列中,研究人员发现KRAS突变状态与CD47表达呈正相关。
在治疗上,用KRAS siRNA、KRAS(G12C)抑制剂AMG 510或miR-34a mimic破坏KRAS-CD47信号轴可抑制CD47表达,增强巨噬细胞的吞噬能力并恢复先天免疫监测。总的来说,这项研究揭示了活跃的KRAS和先天免疫逃避之间的直接机制联系,并确定CD47是KRAS介导的免疫抑制肿瘤微环境的主要效应因子。
本研究的科学价值体现在以下几个方面:
- 它确定了KRAS在逃避先天免疫监测方面以前未被怀疑的作用。本研究的发现与之前关于KRAS在适应性免疫应答中的作用的发现相补充,表明KRAS突变是肿瘤免疫逃避的核心。因此,抑制KRAS信号可以导致癌症细胞更容易受到T细胞(适应性免疫)和巨噬细胞(先天免疫)的免疫攻击,这可能有助于KRAS抑制剂在体内的整体抗肿瘤作用。
- 建立了KRAS突变状态与CD47表达的正相关关系肺腺癌病人。抗cd47抗体最近已进入III期临床试验然而,治疗反应的预测性生物标志物仍然缺乏。KRAS突变状态可作为患者选择的生物标志物,以增强抗cd47免疫治疗的有效性。
- 它提供了初步的临床前证据支持联合治疗使用KRAS抑制剂和抗cd47抗体。联合KRAS(G12C)抑制剂AMG510/MRTX849和PD1/PD-L1抑制剂的临床试验已经在进行中。KRAS抑制剂和抗cd47抗体的组合很可能为KRAS驱动的癌症患者提供协同效益。
这篇论文发表在临床研究杂志.
更多信息:胡欢欢等,KRAS信号通路在肺腺癌中通过激活CD47来规避先天免疫监测,临床研究杂志(2022)。DOI: 10.1172 / JCI153470