便携式和可负担得起的全光学系统,用于测试芯片上的实验室人类心脏

生物工程师最近采用了人类诱导的多能干细胞衍生心肌细胞(hiPSC-CMs)作为人类心脏的模型。这种“芯片实验室”的人类心脏可以用来研究这些心脏波对各种刺激的反应中断,使用患者自己的重编程细胞。光学成像可以帮助可视化波浪,尽管它非常敏感高速摄像机而每一个都很昂贵,大约要花费10万美元。
在这种背景下,由乔治华盛顿大学Emilia Entcheva领导的研究人员现在开发了一种便携式、低成本的全光学宏观测绘系统心脏电生理学.他们没有使用电刺激,而是使用光(光遗传刺激)在hiPSC-CMs中触发电压、钙波和机械收缩。
“光遗传学使用光敏蛋白质从在人类细胞中基因表达的藻类到以类似于使用电脉冲实现的方式来控制它们。然而,光的利用能够以非接触的方式同时刺激许多样品,而不需要任何布线。这在电脉冲中是不可能实现的,”Entcheva解释道。他们的研究最近发表在生物医学光学杂志.
为了使他们的系统负担得起,研究人员使用了便宜的高速机器视觉CMOS摄像机,价格比通常用于此目的的科学CMOS摄像机低100倍。实验室博士后、第一作者Yuli Heinson构建了一个多摄像机系统,利用led和现成的组件进行刺激和控制。
使用倾斜LED照明可以识别局部无染料信号的小机械收缩,同时成像厘米尺度的区域。Entcheva说:“这可能代表了一种基于干扰的检测机制。”整个可重构的多摄像机装置的成本不到15,000美元,外形尺寸较小,即比传统设计更小,并且便于携带。
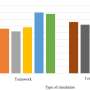
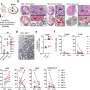
一旦系统就位,研究人员广泛量化了不同实验条件对测量波参数的影响。使用不同功率的照明,他们表明hiPSC-CMs的电和光遗传刺激是等效的。
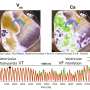
然而,由于钙波是使用绿色光激发荧光传感器成像的,而且这种光也可能部分激活基于蓝色光的光遗传致动器,研究人员发现,需要使用极低的照明来不改变钙波速度。电压和钙图在受控的电或光遗传起搏条件下提供了类似的信息。这些波的速度随温度和所用实验溶液的类型而变化。
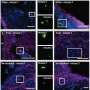
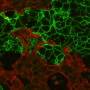
最后,研究人员介绍了他们的系统的潜在应用。该系统显示,检测传导变化由于药物靶向细胞-细胞耦合。此外,它的透光模式可以重新配置为外延照明设置,用于成像较厚的样本,如心脏图像切片或整个心脏的表面。
新型全光学装置的优点不仅限于上述演示。在设置设计中,多个光学传感器和执行器的组合可以处理光谱拥塞并避免参数失真。这项新技术可以帮助表征hiPSC-CMs以及进一步的基础和转化性心律失常研究,该论文的合著者Julie Han在她的博士研究期间正在进行这项工作。此外,它还可以在不久的将来为其他实际医学应用打开大门。
“患者来源的细胞能够对最合适的药物组合进行个性化测试。因此,开发的技术可以帮助确定患者的最佳治疗方案,促进有效和安全的治疗,”Entcheva说。
此外,任何药物开发都要经过临床前心脏毒性安全测试。提出的廉价系统可以帮助设计出更好、更快的检测方法,从而挽救生命和金钱。它的紧凑性允许在大型药物相关实验室以及资源较低的环境中部署,例如学术实验室和发展中国家,”她总结道。