研究重新认识移植物抗宿主病
新的研究挑战了供体干细胞移植如何导致移植物抗宿主病(GVHD)的流行假设,并提供了一种可指导新疗法发展的替代模型。
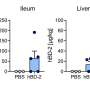
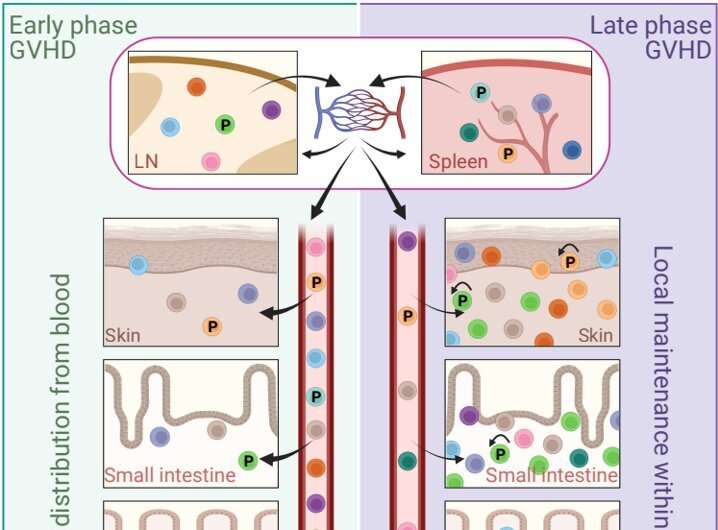
今日出版于免疫力该研究在小鼠模型中显示,通常影响皮肤、肠道和肝脏的GVHD是由供体T细胞维持的,这些T细胞在移植后很快就在这些组织中播下种子,而不是像之前认为的那样,由血液中不断补充T细胞来维持。
“这项研究改变了人们对GVHD的看法,”共同资深作者Warren Shlomchik博士说,他是UPMC Hillman癌症中心造血干细胞移植和细胞治疗项目的主任,匹兹堡大学医学院医学和免疫学教授。“它提供了关于受GVHD影响的组织中发生了什么事情的重要机制细节,这最终可以为更好的治疗方法的发展提供信息,并为干细胞受体带来更好的结果。”
异基因干细胞移植是指将健康供体血液或骨髓中的干细胞注入受者体内。虽然这种治疗通常可以挽救白血病和其他血液疾病患者的生命,但也有可能导致GVHD,这是一种危及生命的疾病,当供体的异源反应性T细胞攻击受体的健康组织时就会发生。
根据一个被广泛接受的理论,GVHD是由T细胞维持的,这些T细胞不断地从全身的次级淋巴器官(包括脾脏和淋巴结)通过血液迁移到受影响的组织。
然而,一种不同的模型假设,这种疾病是由组织中的T细胞局部维持的,几乎没有来自血液的输入。在这项新的研究中,Shlomchik,主要作者Faruk Sacirbegovic博士,皮特外科研究助理教授,和他们的团队调查了GVHD如何在组织中维持的两种假设。
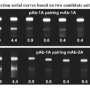
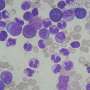
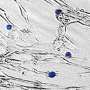
研究人员开发了一种系统来跟踪细胞中的异源反应性T细胞小鼠模型通过标记来预防GVHD单个细胞用独特的标签来创造不同的T细胞“味道”。通过测量标签随时间的变化,他们监测T细胞在哪里移动和复制。
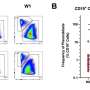
分析表明,每一个组织受GVHD影响的T细胞群独特,每种T细胞风味的频率不同。
“这一发现有力地证明了这种疾病是由每个组织中的T细胞局部维持的,”Shlomchik解释说,他同时也是匹兹堡基金会癌症免疫学主席。“如果组织不断地从循环血液中获得T细胞,那么随着时间的推移,每个组织中T细胞味道的频率应该变得越来越相似——但我们没有看到这一点。”
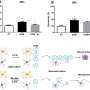
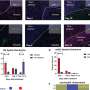
由共同资深作者Thomas Höfer博士领导,他是德国癌症研究中心的部门负责人,海德堡大学理论系统生物学教授,该团队使用数学模型预测祖T细胞在移植后早期播下种子进入受体组织,并分化为致病细胞。
Sacirbegovic接下来进行了一系列实验来证实这一预测,并将这些祖细胞识别为表达Tcf7基因的T细胞。
Sacirbegovic说:“我们认为祖T细胞在目标组织中寿命很长,对维持GVHD至关重要。”“在最初的播种阶段之后,疾病主要在组织内部持续,没有血液中新的T细胞的大量输入。”
干细胞受体通常使用免疫抑制剂来预防和治疗GVHD。因为这些强有力的药物有系统地抑制免疫系统此外,它们还会降低对感染的免疫力,并有其他副作用。
根据研究人员的说法,这项研究的见解最终可能会导致针对GVHD的新的靶向疗法。
“现在我们知道了祖先的身份细胞我们可能能够防止它们在移植后早期形成,或者在它们形成后直接针对它们,”什洛姆奇克说。“研究结果还表明,在组织本身治疗GVHD将是有效的,尽管针对皮肤以外的组织仍然是一个挑战。”
有了更好的方法来最大限度地降低干细胞移植后GVHD的风险,该程序可以更广泛地用于治疗更广泛的疾病,包括血液疾病,如血液疾病镰状细胞性贫血以及狼疮和多发性硬化症等自身免疫性疾病。
对这项研究做出贡献的其他作者有Matthias Günther,博士,Alessandro Greco, M.S和Wang,博士,都是德国癌症研究中心和海德堡大学的;赵大强,医学博士,博士,周孟,博士,Sarah Rosenberger, m.s., Martin H. Oberbarnscheidt,医学博士,博士,所有皮特大学;洛桑大学Werner Held博士;以及耶鲁大学的Jennifer McNiff医学博士和Dhanpat Jain医学博士。
更多信息:Warren D. Shlomchik和同事,移植物抗宿主病是由常驻祖细胞样T细胞在靶组织中局部维持的,免疫力(2023)。DOI: 10.1016 / j.immuni.2023.01.003.www.cell.com/immunity/fulltext…1074-7613(23)00013-4