研究人员绘制了阿尔茨海默病中脑细胞的变化
阿尔茨海默病的一个常见症状是大脑中两种蛋白质的过度积累:在细胞内积累的tau蛋白缠结,以及在细胞外形成斑块的淀粉样β蛋白。研究人员不知道这些蛋白质沉积与该疾病的另一个主要特征——大脑神经元死亡——有什么关系。
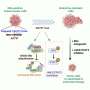
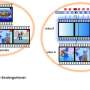
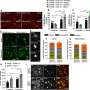
麻省理工学院和哈佛大学布罗德研究所的科学家今天在《科学》杂志上发表了一项研究自然神经科学暗示了这个问题的一些答案。该团队使用他们开发的一种新方法来揭示位于这些蛋白质附近的脑细胞是如何随着阿尔茨海默病小鼠模型的疾病进展而变化的。这项名为STARmap PLUS的技术首次同时绘制了单个细胞的基因表达及其位置,以及完整组织样本中特定蛋白质的空间分布。
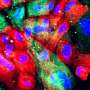
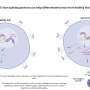
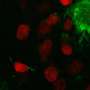
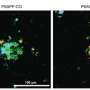
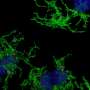
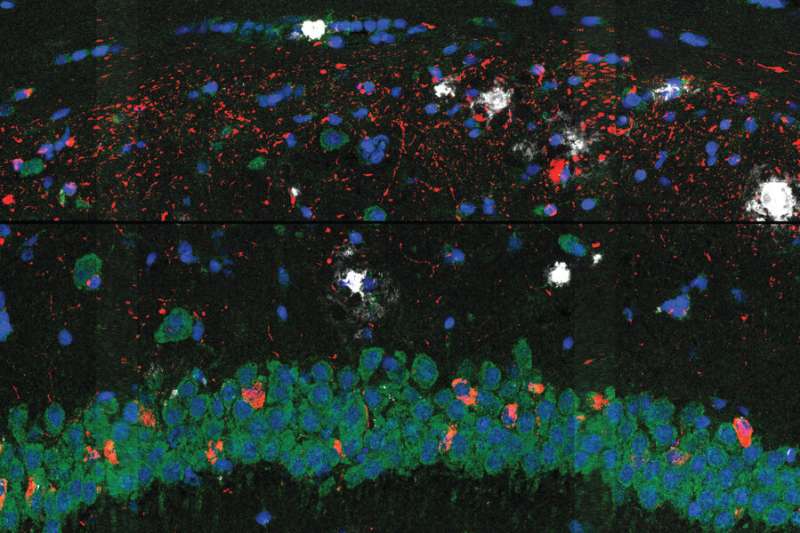
研究人员使用他们的方法进行研究大脑组织来自阿尔茨海默氏症小鼠模型,处于疾病的两个不同阶段,并具有高空间分辨率。在早期阶段,他们观察到大脑中淀粉样斑块的中央核心被一种称为小胶质细胞的免疫细胞包围,这种细胞已知在阿尔茨海默氏症中发挥作用。离斑块更近的小胶质细胞显示出与神经退化.
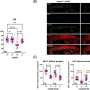
科学家们还发现了其他两种类型的脑细胞的外壳,这些细胞在疾病后期出现。这种核壳结构和蛋白质周围细胞基因表达的差异,让科学家们更清楚地了解了细胞对大脑中蛋白质沉积物的反应——有朝一日,这些见解可能有助于科学家评估现有的阿尔茨海默氏症治疗方法,并开发出新的治疗方法。
“从这类研究中,你可以更详细地推断出发生了什么,而不是仅仅从分散的组织样本中观察细胞,这些细胞不再具有它们的空间背景,”该研究的联合高级作者、布罗德学院斯坦利精神病学研究中心的核心成员和联合主任、麻省理工学院神经科学教授摩根·盛(Morgan Sheng)说。“这是转录组学的一个新维度,我认为它将非常有影响力。”
这项研究建立在先前版本的名为STARmap的技术的基础上,该技术由小王开发,他是这项研究的联合高级作者,布罗德的核心研究所成员和Merkin研究员,以及麻省理工学院的化学教授。
Wang说:“这是对STARmap的一个令人兴奋的改进,因为我们现在可以将整个转录组与同一组织切片中的蛋白质共同映射,许多疾病都涉及蛋白质定位和转录后修饰的变化。”
该项目也是与基因泰克科学家合作,由斯坦利中心的共同第一作者领导:博士后胡曾;研究生黄嘉豪;以及访问研究员周浩文。
制作地图
为了使用STARmap PLUS分析组织样本,王的团队使用分子探针检测特定的mrna,并将其放大为DNA序列。他们还使用抗体来标记和识别特定的蛋白质。然后,他们对组织进行化学处理,将DNA和蛋白质固定在凝胶中的原始位置。最后,他们使用原位测序和成像技术,绘制了标记蛋白的三维图谱,以及2700多个基因的表达。
科学家们发现,大脑的炎症反应和小胶质细胞等神经胶质细胞的分化等过程与疾病进展有关。虽然其他研究人员之前已经观察到斑块周围的核壳结构,但新的基因表达数据显示,小胶质细胞更“激活”以触发一种炎症反应离匾更近一点。科学家们说,这意味着小胶质细胞可能在斑块附近激活,可能会召集其他细胞形成斑块周围的外壳,而不是在远处激活,然后移动到更近的地方。了解小胶质细胞何时、何地以及如何激活可能是破译它们在疾病中的作用的重要部分。
Wang说,STARmap PLUS的一个关键优势是它可以从单个样本中收集蛋白质和基因表达信息,从而更容易在高分辨率下对齐和比较不同类型的数据。它还可以检测到比细胞更小的特征,这有助于区分单个细胞,即使它们在大脑中密集地挤在一起。STARmap PLUS也是可扩展的,可以适应于映射其他蛋白质甚至整个转录组。
除了阿尔茨海默氏症
研究人员说,关键的下一步将是使用这种方法来研究人类脑组织样本中的阿尔茨海默氏症的进展。这将有助于确定在小鼠模型中发生的细胞变化在多大程度上代表了阿尔茨海默症患者的过程。
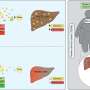
在动物模型中,科学家也可以使用这种方法来回答关于新的治疗策略的问题。例如,如果抗体能够到达并清除斑块,那么附近的小胶质细胞是否会恢复到未激活状态并远离斑块?是消除斑块还是灭活小神经胶质细胞预防附近神经变性?
STARmap PLUS还可以帮助研究人员了解其他疾病,例如癌症,以了解更多,例如免疫细胞如何攻击肿瘤。这种方法也有助于精神分裂症和其他脑部疾病的研究。
“有精神病学的小鼠模型,我们从其他研究中知道,在大脑的不同部分发生了许多不同的事情,”盛说。“能一下子看到这一切真是太棒了。”
更多信息:胡曾等,阿尔茨海默病小鼠模型中单细胞转录状态和组织病理的原位定位,自然神经科学(2023)。DOI: 10.1038 / s41593 - 022 - 01251 - x
本文转载自麻省理工学院新闻(web.mit.edu/newsoffice/),这是一个很受欢迎的网站,涵盖有关麻省理工学院研究、创新和教学的新闻。