研究人员开发了一种促进骨骼生长的新方法
DNA可以以局部和有针对性的方式帮助刺激骨愈合,例如在复杂骨折或手术后严重组织损失后。马丁·路德大学哈雷-维滕贝格(MLU)、莱比锡大学、阿威罗大学(葡萄牙)和弗劳恩霍夫材料与系统微结构研究所IMWS的研究人员已经证明了这一点。他们开发了一种新的工艺,在植入材料表面涂上基因激活的生物材料,诱导干细胞产生骨组织。他们的研究结果发表在该杂志上先进医疗材料.
骨骼是人体再生能力的一个迷人的例子。它们能够恢复全部功能——即使在骨折后——这要归功于它们在骨折部位形成新的弹性组织的能力。“然而,当涉及到复杂的骨折或重大组织损失时,即使是骨头的自愈能力也不够,”MLU制药研究所生物医学材料研究小组负责人托马斯·格罗斯教授解释说。
“在这种情况下,需要植入物来稳定骨骼,替换部分关节,或用可降解材料弥补较大的缺陷。”这种植入物的成功很大程度上取决于它们融入骨头的程度。近年来,通过在植入物表面涂上生物活性材料来激活骨细胞和间充质细胞来支持这一过程干细胞.
间充质干细胞能够生成不同类型的组织,但激活它们以特异性地再生骨骼可能特别具有挑战性。在这种情况下,细胞外基质起着关键作用。“组织之间骨细胞是由胶原蛋白和硫酸软骨素等组成的,”格罗斯解释说。
“它可以被人为复制,并应用于植入物表面,使其具有生物活性。”这确保了植入物被更好地吸收,并且不太可能被身体排斥。也可以在人工细胞外基质中加入药物和激活剂来刺激骨生长。其中一种激活剂是BMP-2蛋白,它已经被用于脊柱融合或治疗复杂的、无法愈合的骨折。然而,研究表明,所需的高剂量BMP-2可导致失控骨组织周围肌肉的形成以及其他不良的副作用。
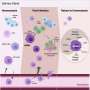
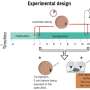
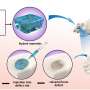
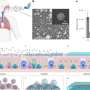
因此,来自哈雷、莱比锡和阿威罗的研究人员提出了一种更有针对性地刺激干细胞的方法,其副作用显著减少。他们关注的一件事是增强细胞外基质的设计。他们使用一种特殊的逐层技术将生物材料应用到植入物上。这使得他们能够在纳米水平上控制其成分、结构和性能。Thomas Groth解释说:“这是一个复杂的过程,我们在MLU与Fraunhofer IMWS合作完善了这个过程。”
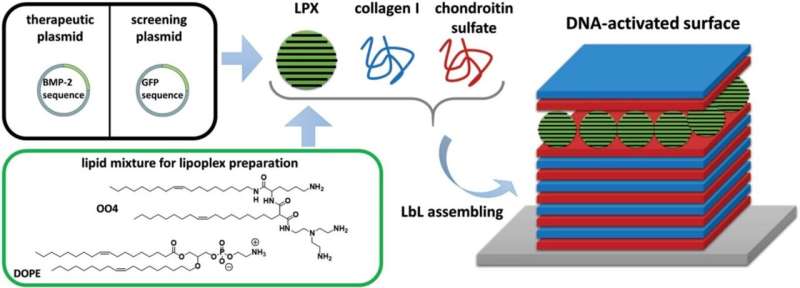
纳米级的设计需要使生物材料功能化;在这里,他们依靠来自莱比锡的同事克里斯蒂安博士Wölk的专业知识。他没有将大量的BMP-2直接整合到生物膜中,冒着不受控制的释放的风险,而是将DNA片段打包到脂质纳米颗粒中,作为运输容器。只有在植入物DNA才会迁移到骨组织的细胞中并刺激它们产生BMP-2。这反过来又激活了骨形成干细胞。
“模仿细胞外基质作为一种薄膜表面涂层,并用纳米颗粒将其功能化是制药材料研究的一个里程碑,”托马斯·格罗斯解释说。“DNA可以有针对性地释放,并在时间和位置上限制对组织生长的刺激,而不会引起不良的副作用。”
根据Groth的说法,这种方法从根本上也适用于信使rna的运输,从而扩大了再生医学的可能性——不仅仅是在医学领域骨形成,也用于其他治疗应用。
更多信息:Catharina Husteden等人,基于细胞外基质成分作为局部基因传递系统的Lipoplex功能化薄膜表面涂层控制成骨干细胞分化,先进医疗材料(2022)。DOI: 10.1002 / adhm.202201978