一场古老的战争:科学家发现了疟疾如此狡猾的敌人的原因
恶性疟原虫是一种寄生虫,会导致人类最致命的疟疾。它是一种逃避疾病的高手,所有针对有效和持久疫苗的尝试都未能成功。现在,Chan Zuckerberg Biohub - San Francisco (CZ Biohub SF)和UC San Francisco (UCSF)的研究人员使用一种复杂的方法来描述抗体如何对所有寄生虫的大约5400种蛋白质做出反应,绘制了第一张人类对恶性疟原虫免疫反应的高分辨率地图,为这种寄生虫成为持久性病原体的原因提供了深入了解。
一项研究发表在eLife3月10日,研究人员采用一种复杂的方法将组成恶性疟原虫的蛋白质分解成我们所能识别的片段免疫系统然后让他们接触198名乌干达成人和儿童的血液。结果表明,抗体与许多恶性疟原虫区域结合,而这些区域不会产生长时间的抗体反应,这是一种明显的“转移策略”,迫使免疫系统产生较短时间的反应。
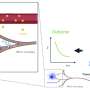
该研究的共同高级作者、CZ Biohub SF总裁乔·德里西说:“在免疫逃避方面,疟疾是专业的。”“但我们的新发现表明,与使用隐形技术不同的是疟疾寄生虫基本上是在上演一场烟花表演,分散免疫系统的注意力,让它追逐最终无助于形成长期保护的目标。”
老练的敌人
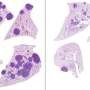
至于为什么持久的疟疾疫苗如此难以获得,专家指出了寄生虫生命周期的复杂性。恶性疟原虫在通过人体它首先像单细胞蠕虫一样在血液中滑行,然后在肝脏细胞中繁殖,然后爆炸成循环系统反复吞噬红细胞内容物作为繁殖的燃料。
这种寄生虫在基因上也很复杂,有数百种蛋白质被认为是用于免疫逃避的。寄生虫的蛋白质还具有大量的简单重复序列,这让科学家们困惑了几十年。
面对如此复杂的敌人,我们的自然免疫反应和创造疫苗的努力都不足为奇。生活在疟疾传播地区的人们只有在一生中多次重复接触疟疾,才会在感染寄生虫后不再生病——有时这还不够。
培养免疫力需要很长时间,这让儿童面临的风险尤其大。更重要的是,来之不易的免疫力很快就会衰退——离开高传播地区的人很可能会失去保护,并在返回时再次生病。
开发自然免疫力面临的这些挑战已经转移到疫苗工作上。被称为RTS,S的疫苗是第一种被批准用于治疗疟疾的疫苗,它需要连续注射四次,对严重疾病的有效性仍然只有30%左右,而且它所提供的保护在短短几个月后就会逐渐减弱。
“关于对疟疾的免疫力是如何形成的,我们还有很多不知道的地方,”加州大学旧金山分校的医学教授、这篇新论文的共同高级作者布莱恩·格林登(Bryan Greenhouse)说。“这在很大程度上是因为缺乏全面表征免疫系统反应的工具。但我们在这里开发的新方法将有助于缩小这一差距。”
绘制免疫反应
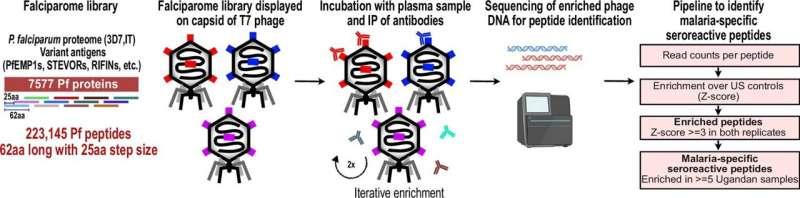
为了更好地理解为什么开发疟疾免疫如此困难,Biohub SF和UCSF的研究人员利用了一种名为PhIP-Seq的强大技术,该技术使他们能够在实验室中分析暴露于恶性疟原虫的人的免疫系统如何对其做出反应。
这种方法包括将构成恶性疟原虫寄生虫的大约5400种蛋白质——疟原虫的“蛋白质组”——切成数十万块,接近我们的免疫系统在寻找病原体碎片时的工作规模。然后,研究人员对病毒进行了改造,使其显示出这些小块——就像挥舞着对方军队旗帜的士兵一样——并将它们与研究参与者的血液混合在实验室培养皿中。
“我们所做的是创建一个包含疟疾可以显示给我们免疫系统的所有蛋白质成分的图书馆,”德里西说,他也是加州大学旧金山分校的生物化学和生物物理学教授。“我们可以准确地看到我们的免疫系统看到了什么,并试图弄清楚它是如何做出反应的。”
现在,研究人员可以分析哪些寄生虫片段触发了人体血液中的抗体来对抗这种疾病。如果免疫系统之前遇到过一个块并产生抗体,那么抗体应该在PhIP-seq平台上对这些块显示出反应性。
正如预期的那样,从对照组的美国成年人中收集的样本,大部分人可能从未接触过疟疾,对寄生虫的蛋白质块几乎没有反应。但当研究小组观察乌干达人捐献的血液时,他们发现了有趣的模式。
乌干达人的血液中含有对艾滋病多种成分的抗体疟疾寄生虫但最常见的是被称为“重复元素”的蛋白质块。重复元件是蛋白质中组成蛋白质的氨基酸序列不断重复的区域,被认为在蛋白质的功能中起不到什么作用。
奇怪的是,对重复元素的反应很大程度上取决于曝光量。生活在疟疾暴露率极高的乌干达儿童——平均每年被感染蚊子叮咬49次——对这些重复元素的反应比生活在中等暴露率地区的儿童(每年被感染蚊子叮咬5次)高出大约两倍。
但是,对这些重复元素的反应性随时间的推移而减弱,而对非重复区域的反应性减弱得更厉害。这一明显的差异表明,虽然针对这些重复元素的抗体主导着对疟疾的免疫反应,但这种反应是短暂的,比针对非重复区域的反应消失得更快。
这项新研究的主要作者、加州大学旧金山分校生物化学和生物物理学博士后学者马杜拉·拉加万(Madhura Raghavan)说:“在建立长期防御时,这些重复往往不是很好的目标。”“免疫资源是有限的,就疟疾而言,我们的身体似乎在创造自然免疫力的目标上犯了重大错误。”
德里西表示同意,并补充说:“我们的免疫系统会立即行动起来对付这些诱饵。这是一种分心,让身体错过了下一次真正有帮助的防御机会。”
这些发现可能为疫苗开发提供了重要的教训,疫苗开发通常依赖于模仿人体自身的免疫防御,而不必评估其有效性。事实上,RTS,S疫苗使用恶性疟原虫重复元件作为它的目标——这可能是它的低持久性的解释。
有了新的恶性疟原虫蛋白质组库,生物中心的研究人员计划继续测试乌干达人对疟疾的免疫反应,接下来研究这些反应如何随着时间的推移和不同程度的暴露而变化。他们预计,更多的数据最终将引导他们找到寄生虫蛋白质的特定成分,这些成分可能是引发更有效治疗的关键免疫反应通过接种疫苗。
Greenhouse说:“不幸的是,疟疾对许多人来说只是日常生活的一部分,免疫是唯一能让他们免于持续生病或死亡的东西。”“如果我们想有机会开发出一种有效的、拯救生命的疫苗,我们就必须继续努力,更好地了解这种免疫力。”
更多信息:Madhura Raghavan等人,恶性疟原虫中含有重复抗原的抗体在自然疟疾感染的儿童中是暴露依赖的,寿命短,eLife(2023)。DOI: 10.7554 / eLife.81401