翻译后修饰药物相互作用的综合检测技术
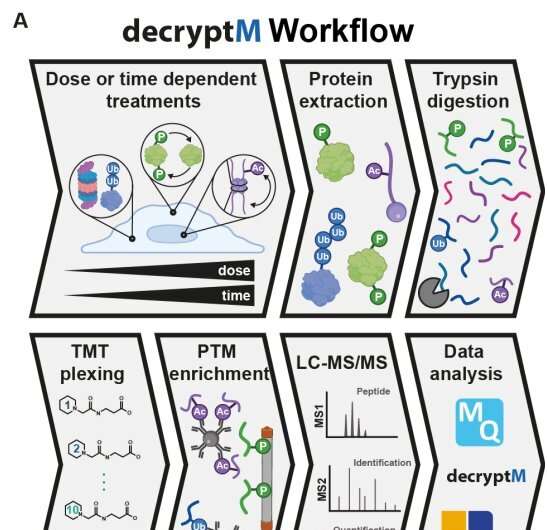
由慕尼黑工业大学领导的一个由37名科学家组成的研究团队开发了一种以时间和剂量依赖的方式检查药物诱导的翻译后修饰(PTMs)的方法。
这项研究发表在该杂志上科学,详细介绍了一种更接近模拟药物蛋白与细胞内蛋白质相互作用时细胞内发生的事情的方法。翻译后修饰(PTMs)是影响蛋白质结构和动力学的加工事件。
因为a的结构蛋白质是否具体到其功能,修改后能显著改变生物过程大多数药物都是这样设计的。虽然药物/细胞蛋白质相互作用已经被普遍理解,但这种相互作用在治疗过程中(时间和剂量依赖)是如何发生的,这是一个尚未得到充分研究的方面。
蛋白质组学分析方法,称为解密tm,涉及用增加浓度的药物处理细胞,并量化数千种药物- ptms,以揭示靶点接合和药物作用机制。
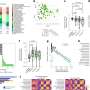
在这项研究中,decryptM分析应用于31个抗癌药物在13个细胞系.该方法获得的数据代表了180万个具有剂量-反应曲线的定量细胞药物分析,在11982个蛋白质上检测到124,660个调节磷酸化肽,在3,006个蛋白质上检测到9,173个泛素化肽,在1,377个蛋白质上检测到2,478个调节乙酰化肽。
大多数PTMs不受大多数药物的调控,这对于了解每种药物正在使用或可能遗漏的通路是有价值的信息。
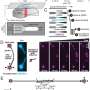
在两种蛋白酶体抑制剂药物bortezomib和carfilzomib的情况下,decrypttm数据显示,随着时间的推移,药物作用变得更强,并提示参与增加的调节磷酸化位点可能是一种机制。
研究还发现,不同的组蛋白去乙酰化酶抑制剂(抗癌药物)具有不同的激活时间,并且药物的特定靶点比其他药物更有效。这类信息可以极大地帮助那些希望提高现有药物有效性的研究人员。
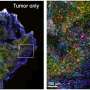
研究人员还使用decryptM配置文件查看了多种乳腺癌细胞类型。不同癌细胞中的信号通路可能有强烈的分歧,解密tm分析揭示了药物相互作用的细胞系特异性特征。例如,一种抗癌药物在两种测试的细胞类型中调控数百个磷酸肽,但在另一种细胞类型中仅调控5个。这正是医生或药物研究人员想要了解的药物/细胞类型相互作用信息。
这项研究强调了目前这种方法的一些局限性。如果一种药物可以作用于具有相似效力的多个靶点,则很难将结果数据归因于特定的靶点。不过,这使得decryptM概要文件成为更多实验的有力起点。
作者设想,解密tm档案可以用于监测并最终预测药物一旦足够的药物和细胞系统被分析,体内反应。此外,将decryptM的抗癌药物配置文件与癌症患者PTM档案可能成为个性化和循证治疗建议的重要工具。
更多信息:Jana Zecha等人,通过剂量和时间分辨蛋白质组学解密药物作用和蛋白质修饰,科学(2023)。DOI: 10.1126 / science.ade3925
©2023科学欧宝app网彩X网络