DNA疗法可以延缓几乎所有ALS患者都会出现的瘫痪
在几乎所有的肌萎缩性侧索硬化症(ALS)患者以及多达一半的阿尔茨海默病(AD)和额颞叶痴呆患者中,一种名为TDP-43的蛋白质从其在细胞核中的正常位置丢失。反过来,这引发了他敏-2的损失,这种蛋白质对神经元的再生和维持它们与肌肉纤维的连接至关重要,对收缩和运动至关重要。
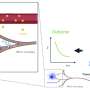
发表在2023年3月16日的科学加州大学圣地亚哥分校医学院医学、神经科学、细胞和分子医学特聘教授、资深研究作者唐·克利夫兰博士及其同事和其他人员领导的科学家团队证明,使用设计DNA药物可以恢复蛋白质编码RNA的正常处理,从而挽救statmin2的损失。
“在小鼠模型中,我们设计了错误处理它们的statmin -2编码rna,就像在这些人类疾病中一样,我们表明,将这些设计DNA药物中的一种注射到大脑周围的液体中脊髓恢复整个神经系统正常的稳态激素-2水平,”克利夫兰说。
克利夫兰被广泛认为是开发了设计DNA药物的概念,这种药物可以打开或关闭与衰老的人类神经系统的许多退行性疾病相关的基因,包括渐冻症、阿尔茨海默氏症、亨廷顿舞蹈症和癌症。
目前,几种设计DNA药物正在针对多种疾病进行临床试验。其中一种药物已被批准用于治疗一种名为脊髓性肌肉萎缩的儿童神经退行性疾病。
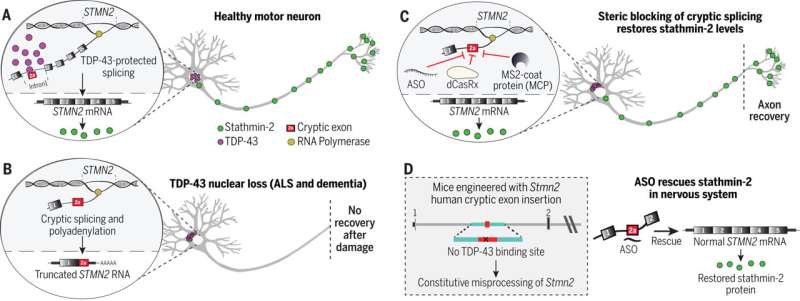
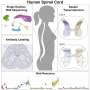
这项新研究建立在克利夫兰和其他人正在进行的关于TDP-43的作用和损失的研究基础上,TDP-43是一种与ALS、AD和其他神经退行性疾病相关的蛋白质。在渐冻症中,TDP-43的丢失会影响运动神经元刺激并触发骨骼肌收缩,导致骨骼肌退化,最终导致瘫痪。
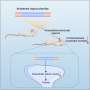
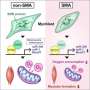
“在几乎所有的ALS病例中,都有TDP-43的聚集,TDP-43是一种蛋白质,在编码许多蛋白质的RNA中间产物的成熟过程中起作用。降低TDP-43活性会导致rna编码statmin -2的错误组装,这是一种维持运动神经元与肌肉连接所需的蛋白质。
“如果没有他敏-2,运动神经元就会与肌肉断开,导致肌萎缩性侧索硬化症的特征——瘫痪。我们现在发现,我们可以用设计的DNA药物模拟TDP-43的功能,从而恢复哺乳动物体内正确的statmin -2 RNA和蛋白质水平神经系统."
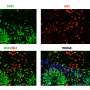
具体来说,研究人员编辑小鼠的基因以包含人类STMN2基因序列,然后将反义寡核苷酸(可以与特定RNA分子结合的一小段DNA或RNA,阻止它们制造蛋白质或改变其最终RNA组装方式的能力)注入脑脊液。注射纠正了STMN2前mrna的错误处理,并恢复了完全独立于TDP-43功能的statmin -2蛋白表达。
“我们的研究结果为通过维持statmin -2来延缓ALS患者瘫痪的临床试验奠定了基础蛋白质克利夫兰说。
更多信息:Michael W. Baughn等,STMN2隐式剪接-多聚腺苷酸化机制及其对TDP-43蛋白病的校正,科学(2023)。DOI: 10.1126 / science.abq5622