修改信使RNA可能为阿尔茨海默病提供一个新的靶点
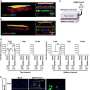
根据3月7日发表在开放获取杂志上的一项新研究,减少关键信使RNA的甲基化可以促进巨噬细胞向大脑的迁移,并改善小鼠模型中的阿尔茨海默病症状公共科学图书馆生物学作者是中国陕西西安空军医科大学的张锐。该结果阐明了外周免疫细胞进入大脑的一条途径,并可能为治疗阿尔茨海默病提供一个新的靶点。
阿尔茨海默病发展的一个假定触发因素是大脑中蛋白质、细胞外淀粉样β斑块的积累。小鼠体内高水平的β -淀粉样蛋白会导致神经退行性变和类似人类阿尔茨海默病的认知症状,减少β -淀粉样蛋白是开发新治疗方法的主要目标。
摆脱淀粉样蛋白的一个潜在途径是迁移的血液髓细胞进入大脑,并成熟为巨噬细胞,巨噬细胞和常驻的小胶质细胞一起,可以消耗淀粉样蛋白。这种迁移是一个复杂的现象,由多个相互作用的参与者控制,但一个潜在的重要因素是细胞内信使RNA的甲基化骨髓细胞。
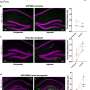
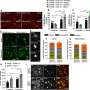
最常见的mRNA甲基化类型被称为m6A,是由METTL3酶进行的,因此作者首先询问髓细胞中METTL3的缺乏是否对阿尔茨海默病的认知有任何影响小鼠模型.他们发现,服用了该药物的小鼠在各种认知测试中表现得更好,当它们阻止髓细胞向大脑的迁移时,这种效果可能会被抑制。
mRNA甲基化降低如何促进髓细胞迁移?作者阐明了一种复杂的机制。通过分析mRNA表达模式和其他技术,他们发现METTL3的缺失降低了一个关键m6A阅读蛋白的活性,该蛋白可以识别m6A修饰的mRNA并促进其翻译成蛋白质。这导致了另一种蛋白质的下降,抑制了另一种叫做ATAT1的蛋白质的产生。ATAT1的缺失减少了乙酰基对微管的附着,而这种减少反过来促进了髓系细胞向细胞的迁移大脑,随后成熟为巨噬细胞,清除增加淀粉样β蛋白,并改善小鼠的认知能力。
“我们的研究结果表明,m6A修饰是治疗阿尔茨海默病的潜在靶点,”作者总结道,同时注意到阿尔茨海默病中的这种途径疾病有待探索。由于mRNA甲基化对广泛的下游靶标具有根本影响,因此在这一途径中有效的药物开发可能需要进一步向下游移动以避免不必要的影响。
更多信息:单核细胞来源的巨噬细胞中m6A甲基转移酶METTL3的缺失改善了小鼠阿尔茨海默病的病理,公共科学图书馆生物学(2023)。DOI: 10.1371 / journal.pbio.3002017