新的SARS-CoV-2靶点可以增强对所有冠状病毒的免疫力
根据今天发表在《柳叶刀》杂志上的一项研究,在SARS-CoV-2病毒中寻找新的治疗靶点的研究人员发现了所有冠状病毒中存在的一个潜在的阿喀琉斯之踵eLife.
这项研究可能有助于开发更强大的抗体药物和疫苗病毒目前导致COVID-19的病毒,也可能预防新冠病毒的出现冠状病毒这可能会导致未来的大流行。
大多数针对COVID-19的疫苗和基于抗体的治疗方法都是通过破坏病毒上的蛋白质突刺和病毒上的ACE2受体之间的相互作用来中和SARS-CoV-2病毒人类细胞,病毒会劫持它进入系统。但是基因突变峰值蛋白质这意味着新出现的SARS-CoV-2变体可以逃避人类抗体反应,因此治疗不起作用,接种疫苗的人会出现突破性感染。解决这一问题的一种方法是针对病毒生存所需且不能突变的部分刺突蛋白进行靶向治疗和疫苗。
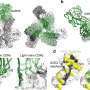
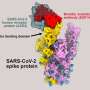
SARS-CoV-2刺突蛋白由两个亚单位组成,称为S1和S2。S1亚基包含一个与ACE2受体结合的区域,而S2亚基允许病毒与它正在访问的细胞膜融合。刺突蛋白的大多数突变都会影响它的S1结构域,但S2结构域在所有7种人类冠状病毒中都高度保守,这表明它可能是一个很好的靶点治疗性抗体和疫苗。
美国德克萨斯大学奥斯汀分校的前研究生Rui Silva解释说:“我们知道,在COVID-19感染后会产生s2定向抗体,流感和艾滋病毒中的类似亚单位也会被人体抗体靶向。”Rui Silva与研究生Yimin Huang和高级科学家Annalee Nguyen密切合作领导了这项工作。
“然而,我们对结合S2亚基的抗体知之甚少。在大约7000种已知的抗sars - cov -2抗体中,只有不到5%的抗体与S2结合,只有两类S2结合抗体被详细描述。我们已经发现了第三类S2抗体,它结合了S2亚基的高度保守部分。”
研究小组用相关中东呼吸综合征病毒的S2亚基免疫小鼠,分离出抗体,并收集了该病毒和SARS-CoV-2结合峰值产生的抗体。然后他们进一步分析了最有希望的抗s2抗体。
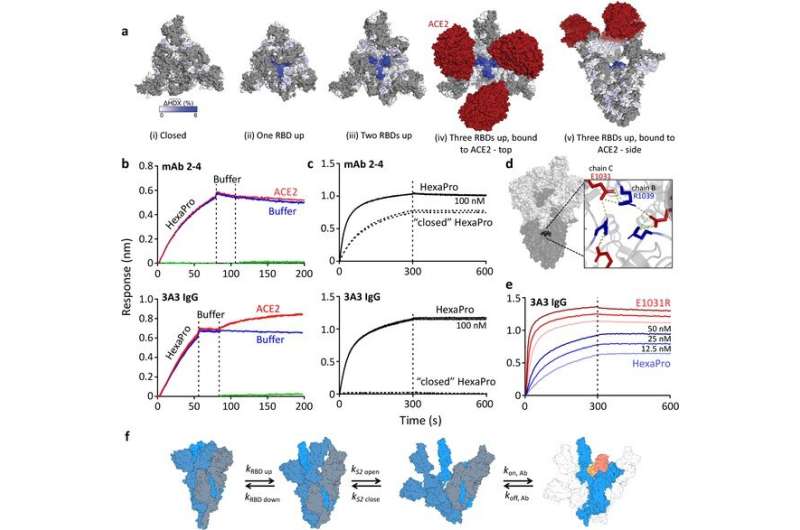
他们发现这种抗体结合S2亚基中的一个铰链,当亚基在病毒与人类细胞膜融合的过程中改变形状时,S2亚基起着至关重要的作用。进一步的分析表明,抗体能否到达与这个铰链(称为表位)结合的点取决于整个刺突蛋白的形状变化动力学;当尖峰与ACE2受体结合时,铰链上的表位就可以被访问。
然后,研究小组进行了一系列实验,以观察靶向这个铰链表位是否对病毒活性有任何影响。他们发现,尽管s2定向抗体可以阻止刺突蛋白融合病毒和人类细胞膜的能力,但它们在完全中和病毒方面的能力较弱。
然而,除了直接中和病毒,抗体也通过触发其他过程间接杀死病毒感染的细胞。在一项实验中,s2定向抗体可以触发人类自然杀伤细胞破坏SARS-CoV-2感染细胞。在另一个实验中,S2抗体导致单核细胞吞噬并摧毁被感染的细胞。这表明,尽管S2抗体可能不够强,无法直接阻止感染,但它们可以用来帮助促进或保护免疫反应。
“我们已经在SARS-CoV-2的S2亚基中确定了一个表位,它在所有致病性冠状病毒毒株中都高度保守,”德克萨斯大学奥斯汀分校化学工程ZD Bonner教授、资深作者詹妮弗·梅纳德总结道。“虽然单独针对这个表位作为一种治疗或疫苗不太可能足够有效,但可以增强对这个表位的获取的治疗策略可以使现有的人类抗体通过其他抗体导向的细胞杀伤过程更有效地促进病毒清除。”
更多信息:Rui P Silva等,所有高致病性冠状病毒刺突蛋白上存在的S2表位的鉴定,eLife(2023)。DOI: 10.7554 / eLife.83710