科学家揭示了一种治疗肝癌的潜在新方法
美国国立卫生研究院和波士顿马萨诸塞州总医院的科学家们发现了一种潜在的治疗肝癌的新方法,这可能会导致一种新型抗癌药物的开发。在对细胞和小鼠进行的一系列实验中,研究人员发现,肝癌细胞中产生的一种酶可以将一组化合物转化为抗癌药物,杀死细胞,减少动物的疾病。
研究人员认为,这种酶可能成为开发新药的潜在靶点肝癌症,也许还有其他癌症和疾病。
“我们发现一种分子可以杀死罕见的细胞肝癌以一种独特的方式,”转化科学家马修·霍尔博士说,他是NIH国家推进转化科学中心(NCATS)这项工作的领导者之一。“它是从筛选中发现选择性杀死人类的分子肝癌细胞.我们做了很多工作才弄清楚,这种分子是由这些肝癌细胞中的一种酶转化的,从而产生了一种有毒的抗癌药物。”
霍尔,麻省总医院的肝癌专家纳比尔·巴迪西博士和他们的同事于3月13日报告了他们的结果自然癌症.
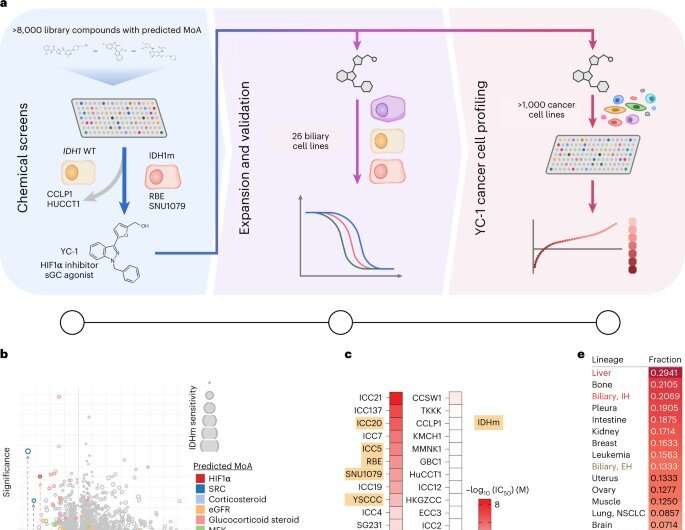
这一发现源于马萨诸塞州总医院和NCATS研究人员的合作。Bardeesy最初研究的是胆管癌,这是一种影响胆管的肝癌。这种癌症的特征是IDH1酶的突变。Bardeesy的团队希望找到可能有效对抗IDH1突变的化合物和药物。通过与NCATS的合作,Hall和其他NCATS的科学家迅速测试了数千种已获批准的药物和实验性癌症药物,以IDH1为靶点,测试它们杀死胆管癌细胞的有效性。
他们发现包括YC-1在内的几种分子可以杀死癌细胞。然而,当他们观察YC-1是如何工作的时,他们发现这种化合物不会影响IDH1突变。
马萨诸塞州的研究人员表明,肝癌细胞会产生一种名为SULT1A1的酶。这种酶激活了YC-1化合物,使其具有毒性肿瘤细胞在癌细胞培养和肝癌小鼠模型中。在YC-1治疗的动物模型中,肝脏肿瘤要么生长减慢,要么缩小。相反,研究人员发现,在癌细胞缺乏这种酶的动物体内,用YC-1治疗的肿瘤没有变化。
研究人员检查了化合物和药物库的其他药物筛选结果数据库药物与SULT1A1活性相关。他们还查看了美国国家癌症研究所的大型抗癌化合物数据库,以寻找更多的可能性来测试它们与维生素c的活性酶.
他们发现了几种依赖于SULT1A1的化合物的肿瘤杀伤活性。使用计算方法,他们预测其他化合物也可能依赖于SULT1A1。
“一旦我们发现SULT1A1激活了YC-1,我们就会问,“还有哪些化合物是活性的,可以通过相同的机制杀死细胞?”霍尔说。“我们能否确定其他正在开发的化合物,并证明它们也因为SULT1A1的激活而具有活性?”答案是肯定的。我们发现了其他与YC-1具有相同作用机制的化合物。”
科学家们认为,这些发现对开发新产品具有更广泛的意义抗癌药物.Bardeesy说:“我们认为这些分子有潜力成为一类尚未开发的抗癌药物,这些药物依赖于SULT1A1的抗肿瘤活性。”
研究人员将YC-1和类似的分子视为开发化合物的原型,这些化合物可以有效对抗细胞上的重要蛋白质。修改这些分子的不同部分可以使它们对这些蛋白质更具特异性。研究人员指出,创建了一个“sult1a1激活分子工具包”,可以影响许多不同的目标。
这样的工具箱由数百个已知分子组成。理论上,该工具包涵盖了许多类型的酶,称为硫基转移酶,它们在身体的不同组织中活跃。例如,除了SULT1A1外,人类磺基转移酶SULT4A1在大脑中是活跃的。它可以激活工具箱中的一个分子子集。这可能有助于开发针对脑癌的药物。
Bardeesy说:“我们知道依赖sult1a1的药物已经被发现。”“我们的研究结果表明,可能还有其他依赖于sult1a1的化合物,具有不同的靶标范围。在细胞上识别这些化合物和靶标可能对开发其他类型的小型细胞具有潜在意义分子药物,不仅仅局限于这些癌症。这可能成为治疗某些疾病的新方法。”
更多信息:Lei Shi等,sult1a1依赖的烷基化物磺化是肝癌的谱系依赖易感性,自然癌症(2023)。DOI: 10.1038 / s43018 - 023 - 00523 - 0