研究表明对多囊肾疾病的基因治疗途径
常染色体显性遗传性多囊肾病(ADPKD)是最常见的致命遗传疾病有几百万人仅在美国遭受的条件。没有治愈,但是新的研究可以开门的新基因疗法治疗疾病的大多数情况下。
几十年来,研究人员已经知道PKD1基因的突变,这编码polycystin-1 (PC1)蛋白质,在大约80%的情况下可以导致疾病。然而,蛋白质是太大而不能被修改基因治疗策略。
劳拉Onuchic领导的研究小组,医学博士,博士后研究人员在耶鲁的细胞和分子生理学和迈克尔·卡普兰,医学博士,博士,椅子和C.N.H.长教授的细胞和分子生理学和细胞生物学教授发现,只是一小块这种蛋白质可能防止疾病的关键。这一发现可能导致机会开发一种新的疗法。3月30日在团队公布了调查结果自然通讯。
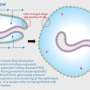
“我们的研究表明,一个小片段的PC1蛋白质只从尾端的200个氨基酸,蛋白质是足以抑制疾病小鼠模型,”卡普兰说,他是这项研究的主要研究者。“我们的工作将提供洞察潜在疾病的机制多囊肾疾病和揭示新的发展途径治疗。”
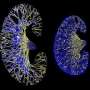
ADPKD是一个遗传性疾病影响在1000人左右。影响肾脏囊肿生长在数量和规模发展。每个肾脏大约有一百万肾元。障碍,在过去的几十年里,这些肾元发展成大,充满液体的囊肿,排挤正常组织。随着时间的推移,这可以压缩和降解的功能部分肾脏,导致肾功能丧失。
“到那个时候,病人的肾脏非常庞大时可以一个足球大小的,“Onuchic说,他是该研究的第一作者。相比之下,一个正常的肾脏在拳头的大小。
大约一半的那些疾病会经历肾功能衰竭需要透析或肾移植。此外,它可以从父母传递给后代一个父是乙肝病毒携带者,一半的孩子可能会受到影响。“那么,你有所有这些大家庭多人携带情况,”她说。
一年多前,Stefan Somlo领导的研究小组,医学博士C.N.H.长期的医学教授(肾脏学)和遗传学教授发现,如果PC1蛋白在小鼠模型,肾脏开始扩大。重新蛋白质表达后,肾脏恢复正常。
“他们做了一个非常漂亮的实验显示,在多囊肾疾病的小鼠模型,这些动物获得巨大肾囊肿,即使这些囊肿已经开发,将恢复正常蛋白的表达使囊肿消失,”卡普兰说。
“这是一个问题治疗策略在4300年,这种蛋白质氨基酸长,”Onuchic补充道。“这是基因传递太大。”The solution, Onuchic and Caplan say, may be to bring gene therapy for ADPKD down to a manageable scale.
研究人员利用基因疗法来的序列编码的基因的兴趣和期望的细胞中表达。这通常涉及到病毒载体。”木马病毒可以提供您感兴趣的基因到细胞需要它,但这些病毒只有一定数量的房间在他们的鼻子”Caplan说。
因为PC1蛋白质是巨大的,这带来了一个问题治疗多囊肾疾病。“PC1太大,适合大多数基因治疗载体的大众甲壳虫,但现在这200氨基酸可以在杂物箱里。”
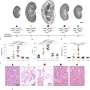
在新的研究中,研究小组使用了小鼠模型转基因,他们已经允许他们关掉基因与多囊肾疾病有关。换句话说,他们在这些模型通过创建基因诱导疾病的突变小鼠的基因组。因此,模型开发的囊肿。
然后,团队打开200氨基acid-long片段的表达的蛋白质。“想象一下翻转一个灯的开关一盏灯熄灭,灯亮了,”卡普兰说。“我们关闭正常多囊肾病基因和打开这个小块的蛋白质的表达。”
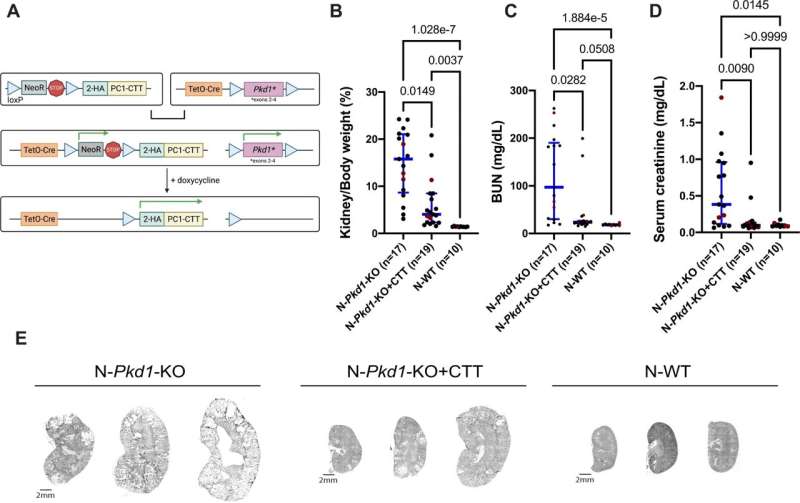
研究小组发现,这大大减少了囊肿的大小。“尽管我们摆脱了完整的长度PC1蛋白质,这通常会导致重大的囊性疾病,就打开这个小块足以抑制疾病,”他说。
此外,研究小组公布线索背后的机制为什么这一小块自己就足够了。通过免疫沉淀反应,他们使用一种抗体分离蛋白质,然后用质谱来确定哪些蛋白质相互作用。他们发现线粒体蛋白质称为烟酰胺核苷酸Transhydrogenase(例数十分)与PC1片段。
“从基础生物学的角度来看,这告诉我们,一些全新的什么多囊肾疾病的蛋白质和打开整个大道来研究其正常功能,”卡普兰说。
团队计划继续追求使用基因疗法,最初在老鼠模型中,仅为200氨基酸,希望有一天他们的工作将造福人类。“从治疗的角度来看,这是非常激动人心的,我们希望能够至少减缓疾病进展,“Onuchic说。
更多信息:劳拉Onuchic et al, c端尾polycystin-1抑制囊性疾病的线粒体enzyme-dependent时尚,自然通讯(2023)。DOI: 10.1038 / s41467 - 023 - 37449 - 1