大胆的新疗法交付方法显示最初的承诺作为治疗杜氏肌萎缩症
科学家道格米莱博士与分工的心血管分子生物学在辛辛那提儿童职业生涯致力于揭示骨骼肌发展的最基本的机制。他一直在描述一个领导者如何两个“fusogens”叫做Myomaker Myomerger调解干细胞进入成熟的肌肉细胞构建组织,人类依靠运动,呼吸,和生存。
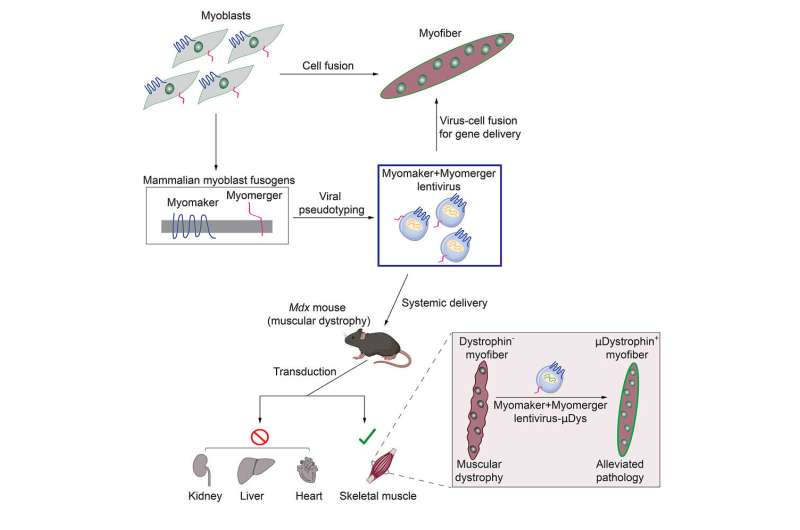
现在,一些基本的发现了米莱和他的同事们正在转化为一个潜在的治疗患者的杜氏肌肉营养不良症(DMD)。最新研究,发表于2023年4月12日,《华尔街日报》细胞表明,在小鼠、修改病毒、工程Myomaker和Myomerger,导致特定的融合肌肉细胞。因此这些病毒可以被用作一个向量提供所需的重要基因肌肉功能突变的模式。
一个关键未知在此之前的工作是蛋白质是否喜欢Myomaker Myomerger,主要功能细胞,甚至可能对病毒。第一作者Sajedah印地语博士的分裂分子在辛辛那提儿童心血管生物学,研究小组的主要成员,来测试这个想法的挑战。
印地语首先设计了一个战略Myomaker和Myomerger病毒和表面显示,他们在培养细胞功能。她继续利用丰富的经验在骨骼肌生物学测试这些小说向量在小鼠的疗效。
“这修改病毒载体似乎是一个有前途的工具,提供一个潜在的终身供应DMD患者的基因缺失,”米莱说。“这个向量的独特优势提供一个显著影响的机会基因治疗无数的肌肉疾病。”
杜氏肌萎缩症是什么?
DMD是一种罕见的和致命的遗传性肌肉疾病的特点是缺乏一个关键membrane-stabilizing叫做肌营养不良蛋白的蛋白质,从而导致渐进式肌肉变性和弱点。DMD罢工主要是男孩,发生在全世界大约每3500个男孩出生。
医生经常诊断疾病3和6岁之间孩子的早期迹象明显的肌肉无力,如延迟能力坐、站、走和困难学习说话。随着时间的推移,DMD变得致命的肌肉变性破坏肺和心脏功能。
没有治愈。然而,寿命延长,生活质量改善了很多物理治疗解决某些症状和药物。一些基因治疗临床试验正在评估使用腺相关病毒(AAV)交付向量,也希望这些策略工作。然而,小说向量,如米莱和他的同事所描述的慢病毒,有可能改善肌肉营养不良治疗的长期交付材料。
修改后的慢病毒在小鼠模型显示的好处
进行大量实验参与这个研究印地语和合作者花了四年才完成。重要的合作者帮助启动项目是本杰明Podbilewicz,从以色列技术研究所的,以色列海法。他们的研究结果包括:
- 证明的骨骼肌fusogens Myomaker Myomerger可以替代病毒fusogens和融合病毒细胞。
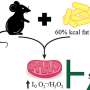
- 具体显示genome-integrating慢病毒(LV)修改携带Myomaker (Mymk)和Myomerger (Mymg)可以有选择地感染骨骼肌提供治疗“货物”。In this case, a miniaturized form of the dystrophin protein called "mDystrophin."
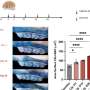
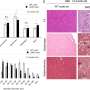
- 记录小鼠模仿人类DMD显示改进这种方法治疗后。最重要的是,横膈膜肌肉治疗有更强的老鼠,突显出潜在的缓解呼吸困难,出现在晚期DMD。
- 证明病毒载体达到肌肉干细胞,这表明潜在的长期受益于治疗。改善功能持续超过六个月在一些治疗肌肉,当信号持续健康的肌纤维生产发现只要11个月之后。
- 进一步揭示,对小鼠的免疫系统没有认识到病毒载体,表明重复剂量如果需要将成为可能。
下一个步骤
需要更多的研究来进一步发展这一发现为治疗DMD患者可能有一天受益。甚至更多的工作还需要确定哪些其他肌肉疾病可能会接受这慢病毒载体。
“我们设想,这一概念,将一个自然发生的过程中肌肉汽车膜,可以彻底改变交付治疗材料骨骼肌改善遗传条件等肌肉萎缩症和条件与肌肉损失和弱点,”米莱说。
更多信息:Sajedah m .印地语等包膜病毒准型与哺乳动物细胞fusogens目标骨骼肌肌原性的基因传递,细胞(2023)。DOI: 10.1016 / j.cell.2023.03.033