我们怎么知道我们的大脑能够修复本身?
是我们的大脑能再生吗?我们能利用这种再生潜力在神经退行性衰老或条件?这些问题引发了激烈的争议在神经科学领域的许多年。荷兰神经科学研究所的一项新的研究显示为什么有冲突的结果,对如何解决这些问题提出了一个路线图。
利用的再生潜力的概念人类的大脑在老化或神经系统疾病代表一个特别有吸引力的替代传统的策略提高或恢复大脑功能,尤其是考虑到目前缺乏有效的治疗策略在神经退行性疾病如阿尔茨海默氏症。
是否人类的问题大脑具有再生的能力或不被激烈的科学辩论的中心多年,最近的研究产生了相互矛盾的结果。一项新的研究从Giorgia Tosoni和Dilara Ayyildiz, Evgenia萨尔塔的监督下在实验室的神经发生和神经退化,批判性讨论并细读之前发布的数据集。怎么可能,我们还没有找到一个明确的答案这个谜吗?
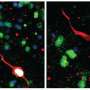
先前的研究中,分裂细胞在后期人类大脑标记,表明新细胞确实可以出现在成人大脑的海马,一个结构,在学习和记忆中起着重要的作用,而且也严重影响阿尔茨海默氏症。然而,其它的研究反驳这些结果并不能检测的产生新的脑细胞。
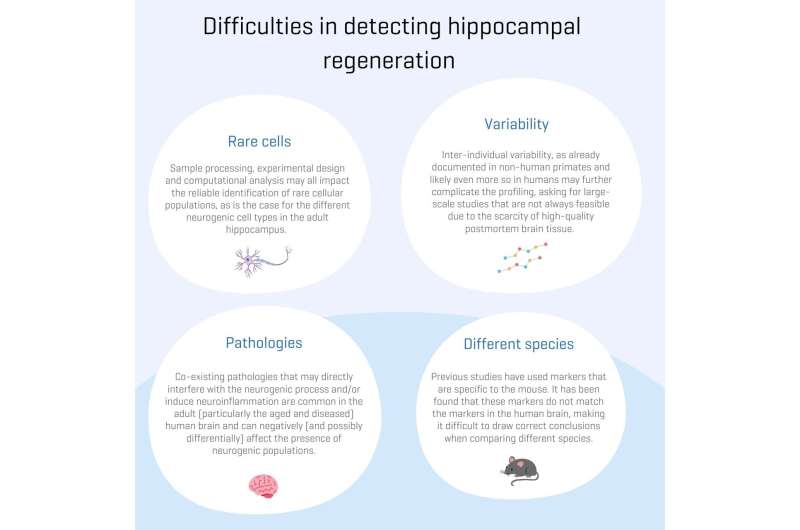
概念和方法论的混杂因素都有可能导致这些看似对立的观察。因此,阐明再生的程度在人类的大脑仍然是一个挑战。
新的先进的技术
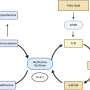
最近的单细胞转录组技术的进步提供了宝贵的见解不同的细胞类型中发现人类的大脑从已故捐赠人与不同的脑部疾病。迄今为止,单细胞转录组技术已经被用来描述人类大脑中罕见的细胞群。除了识别特定的细胞类型,single-nucleus RNA序列还可以探索特定的基因表达谱来解开海马细胞的复杂性。
单细胞转录组技术的出现最初被视为万能的解决争议。然而,最近的单细胞RNA序列研究在人类海马产生了相互矛盾的结果。
两项研究确实发现神经干细胞,第三个研究未能发现任何神经性的人群。这些小说approaches-once失败最终解决争议关于海马再生在人类的存在?我们最终能克服概念和技术挑战,协调这些看似对立观点和发现?
技术问题
在这项研究中,研究人员极度反复讨论以前公布的单细胞转录组数据集。他们警告说,设计,分析和解释这些研究的成人海马可以驳倒的具体问题,都要求概念、方法论和计算调整。由re-analyzing以前公布的数据集,探讨了一系列具体挑战,需要特别注意,将极大地利润从一个开放的讨论。
Giorgia Tosoni说,“我们以前发表单细胞转录组研究和执行分析荟萃分析评估成年神经源性人口能否可靠地确定在不同的物种,特别是当比较小鼠和人类。成年小鼠的神经源性过程是很好和概要文件的不同细胞种群特征是已知的。”
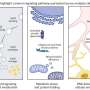
“这些实际上是相同的分子和细胞特征,广泛应用于这个领域也在人类的大脑识别神经源性细胞。然而,由于几个进化适应性,我们希望老鼠和人类之间的神经发生是不同的。我们检查每个神经源性细胞类型的标记,看着标记之间的重叠两个物种的数量。”
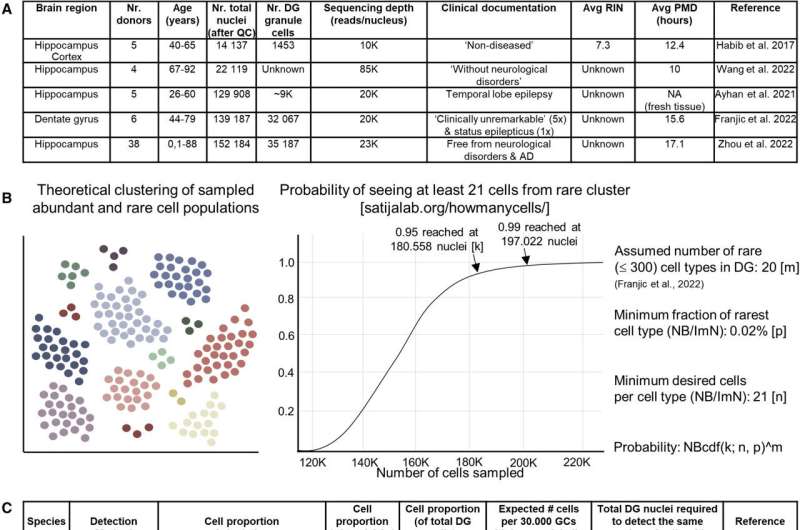
“我们发现很少,如果不,两个之间的重叠,这表明我们长期以来使用的mouse-inferred标记可能不适合人类的大脑。我们也发现,这类研究需要足够的统计能力:如果再生神经细胞发生在成年人的人类大脑,我们期望它是非常罕见的。”
“因此,足够的细胞需要测序以确定这些稀缺,大概是神经性的人群。其他参数也很重要,例如样品的质量。之间的时间间隔的死亡捐赠者和下游加工是至关重要的,因为组织的质量和结果数据随着时间的推移下降。”
再现性是关键
Dilara Ayyildiz说,“当适当地应用,这些新技术提供了一个独特的机会来映射在人类的大脑海马再生和探索细胞类型和状态可能会衰老,最适合治疗干预神经退行性和神经精神疾病。然而,重现性和一致性是关键。做分析时我们意识到一些看似很小,但除此之外非常关键的细节和参数在实验和计算管道,可以在结果产生重大影响,从而影响数据的解释。”
“准确报告是必要的让这些单细胞转录组实验及其分析可再生的。一旦我们重新分析这些先前的研究应用常见计算管道和标准,我们意识到明显的争议在现实中可能是误导:与我们的工作我们建议实际上可能有更多比此前认为的同意。”
这项研究发表在《华尔街日报》神经元。
更多信息:Giorgia Tosoni et al,映射成人海马神经发生与单细胞转录组:协调争议或引发的争论?神经元(2023)。DOI: 10.1016 / j.neuron.2023.03.010