癌细胞是如何侵入其他器官的
来自伦敦大学学院(UCL)、麻省理工学院(MIT)及其合作者的研究人员首次描述了癌细胞如何从血液中逃逸并入侵其他器官的生物力学。
这项研究发表在先进的科学研究发现,多孔性越强、组织越柔软,患病的可能性就越大癌症细胞是强行进入并能够更快地进入,为寻求预防或阻止的研究提供有价值的数据吗癌症转移这是导致癌症死亡的主要原因。
影响肿瘤周围环境硬度的药物,如PAT-1251和pxs -5505,正在试验中临床试验用于尚未扩散的癌症,希望类似的方法可以用于治疗转移性癌症。
实体癌出现在身体的一个地方,称为原发肿瘤部位。转移是指癌细胞脱离原发肿瘤,通过血液或淋巴系统扩散到身体其他部位,从而导致其他器官发生继发性肿瘤。癌细胞从细胞中突围出来的过程循环系统进入其他组织被称为外渗。
大多数癌症研究专注于早期发现癌症并在其扩散之前进行治疗,这已经改善了患者的预后。但是,癌症一旦转移,治疗就会变得更加困难,这一点从转移是绝大多数癌症死亡的一个因素这一事实得到了强调。虽然转移性癌症可以治疗,但不能治愈。
在这项研究中,来自伦敦大学学院和麻省理工学院的研究人员开始更好地了解决定癌细胞如何能够从血液中入侵其他组织的生物力学力量。
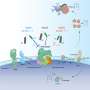
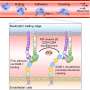
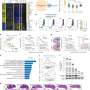
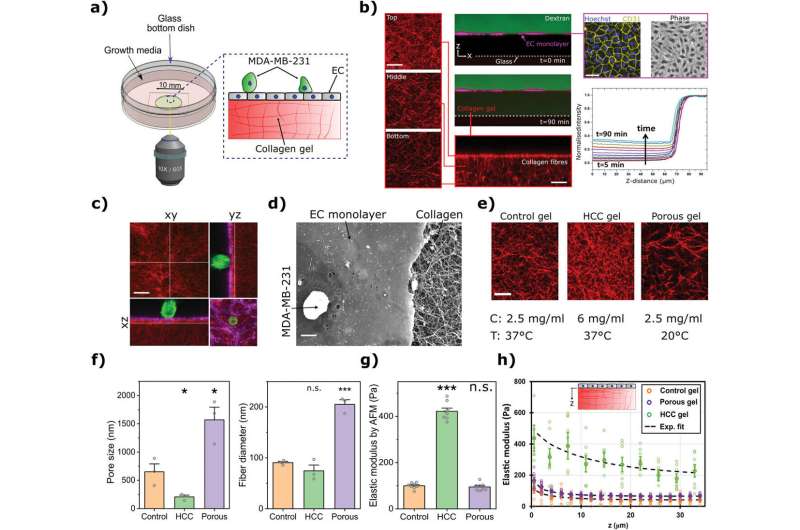
他们创建了内皮细胞(一种将血液与其他组织分开的单细胞层)的体外模型,并将其置于不同制备的胶原蛋白凝胶上,以模拟更坚硬或更多孔的组织。然后将肿瘤细胞引入模型中,观察它们是否能穿透内皮,这需要多长时间,以及从力学角度看它们是如何做到这一点的。
该研究的第一作者Yousef Javanmardi博士(伦敦大学学院机械工程)说:“我们观察到,癌细胞需要附着在内皮细胞上以建立一个固定位置,它们利用这个固定位置来推动和拉动自己穿过这个紧密编织的细胞层,进入组织内部。这就像你被困在厚厚的泥浆中:你需要使用像岩石这样坚固的东西来把自己拉到更坚实的地面上。泥越厚,就越硬。你可能出不去,即使出了,也要花更长的时间。”
这些发现提出了一个问题,即体内特定组织的生物力学特性是否决定了继发性肿瘤的形成。
考虑到以这种方式研究转移的极端困难人体组织下一步将是创建更先进的血管系统三维模型,以便在更好地模仿人类生物学的条件下更详细地观察癌症生物力学。这将允许对药物进行测试,并有望确定用于人体试验的候选药物。
Emad Moeendarbary教授(伦敦大学学院机械工程)是这项研究的资深作者,他说:“看到这种高度跨学科的技术和技术非常令人满意合作研究五年后取得成果。研究转移的挑战是巨大的,物理学家、生物学家、工程师、数学家和肿瘤学家付出了巨大的努力才得出这些发现。这是合作力量的一个伟大广告,我乐观地认为,这些数据将有助于进一步了解癌症转移和开发治疗癌症的药物。”
更多信息:Yousef Javanmardi等,内皮和内皮下基质机制调节癌细胞跨内皮细胞迁移,先进的科学(2023)。DOI: 10.1002 / advs.202206554