基因剪刀找到治疗睾丸癌的靶点
波恩大学医院(UKB)的研究人员现在已经能够阐明睾丸癌顺铂耐药的潜在机制。利用CRISPR基因剪刀,他们确定了NAE1基因是其驱动因子。通过加入NAE1抑制剂MLN4924抑制这种耐药介质,不仅恢复了顺铂的作用,而且对肿瘤细胞有额外的杀伤作用。研究结果已发表在英国癌症杂志.
睾丸癌,也被称为睾丸生殖细胞肿瘤(TGCT),是年轻男性最常见的癌症类型。当用顺铂治疗时肿瘤细胞停止生长,死去。这是因为细胞抑制药物会对遗传信息的载体DNA造成损伤,从而阻止细胞增殖细胞周期.
“警报信号发出‘注意,维修,不要再分割。为了做到这一点,细胞需要所谓的肿瘤抑制基因,这些基因可以准确地抑制这种损伤,并且不释放细胞生长直到它被修复,”UKB病理研究所的Hubert Schorle教授说。这种类型的化疗治愈睾丸癌的机会非常高。然而,在一些患者中,肿瘤产生顺铂耐药,这与生存率降低有关。
过度活跃的基因NAE1会加速细胞分裂
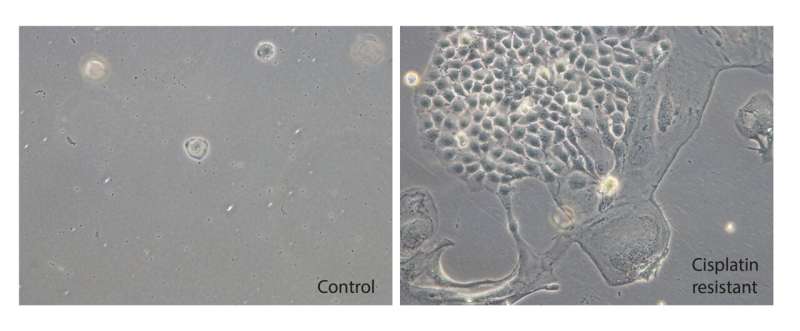
为了弄清睾丸癌中顺铂耐药的原因,波恩研究小组使用了CRISPR基因剪刀。他们用它们来激活睾丸癌细胞中的每个基因一次。然后,他们用顺铂处理转基因细胞培养物,挑出那些存活下来的细胞,结果,细胞抑制药物不再有效。
“通过分析这些细胞的DNA,我们发现了基因剪刀活跃的地方,并能够识别负责顺铂耐药性的基因。除了基因Schorle教授的博士生,第一作者Kai Funke说:“我们已经知道了顺铂耐药性,令我们惊讶的是,我们发现了nee1基因,类泛素化级联的调节器。”
细胞必须能够精确地控制不同蛋白质的种类和数量。除了调节蛋白质的产生,控制蛋白质的靶向降解也很重要。在这里,类泛素化级联标记了注定要降解的蛋白质。
“在DNA损伤的情况下,肿瘤抑制蛋白起到抑制细胞生长的作用,似乎是类泛素化的重要靶点。因此,当nee1基因上调导致类泛素化级联过度活跃时,它们会在更大程度上退化,它们的制动作用也会增强,”Schorle教授解释道,他也是跨学科研究领域(TRA)的成员。波恩大学的"生命与健康"
抑制类泛素化增加睾丸生殖细胞肿瘤的顺铂敏感性
反过来,抑制类泛素化级联导致抑制蛋白的积累,从而停止细胞分裂。随着NAE1抑制剂MLN4924的加入,波恩的研究人员因此观察到对顺铂耐药的睾丸癌细胞对细胞抑制药物的再敏化。结缔组织细胞没有受到治疗的影响,这一事实让人看到了希望,即在应用时可能只有微弱的副作用。
因此,波恩的研究人员强调了MLN4924联合顺铂抑制NAE1的加性作用,作为一种新的治疗方案睾丸癌.“我们在这里首次描述了类泛素化作为睾丸生殖细胞肿瘤的治疗靶点。在其他肿瘤类型的临床试验中,已经对类泛素化的抑制进行了研究。在胰腺癌中,MLN4924也被证明对顺铂Schorle教授说。
更多信息:Kai Funke等人,基因组级CRISPR筛选揭示了类泛素化有助于睾丸生殖细胞肿瘤的顺铂耐药,英国癌症杂志(2023)。DOI: 10.1038 / s41416 - 023 - 02247 - 5