慢性尿路发现背后隐藏的表观遗传机制
发表在微生物学性质,一项对老鼠的研究发现,尿路感染的微生物基础包括本地化的表观遗传改变可以增加感染的可能性更大。
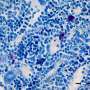
以前的尿路感染(尿)已知未来使患者容易感染,但复发背后的机制并不清楚。华盛顿大学医学院的研究人员在圣路易斯跟进之前的研究,发现微分在小鼠膀胱尿路上皮细胞的变化,导致不同的结果。
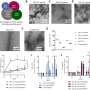
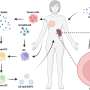
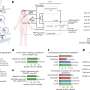
目前的研究中,“Uropathogenic大肠杆菌感染全身的尿路上皮训练免疫影响疾病的结果,“相比移行细胞干细胞(USC)线隔绝老鼠历史的解决或慢性uropathogenic大肠杆菌(UPEC)感染,并发现表观遗传变化,包括染色质易访问性的差异,DNA甲基化和组蛋白修饰。新闻与观点的文章在研究发表在同一本杂志上的研究问题。
一条线索研究人员跟踪调查了,先前的感染导致泌尿道上皮干细胞的变化,持续在许多代细胞培养,表明可能在这些细胞表观遗传修饰。表观遗传修饰不改变细胞的DNA序列,但在如何访问和DNA,因此,基因表达。这些变化可以改变正常的细胞功能,在这种情况下,免疫反应。
他们发现UPEC感染充当epi-mutagen,重组细胞移行细胞的功能活动,导致装修和改建或随后的感染先天反应训练。研究表明直接诱发粘膜细菌感染的特定角色表观遗传变化在粘膜上皮干细胞。
虽然没有提出一个解决方案,对老鼠的研究识别未知的机制,为未来的研究在设计解决慢性尿路。这可能是一个重要和可行的提升我们的知识在这个问题上,目前只提供建议如何使用厕所,擦拭后建议保持生殖器干燥和鼓励大量的酸果蔓汁喝策略来防止再感染。
即使没有目前的治疗方案,这项研究可能是好消息对于那些患有慢性复发感染确认问题是一个epigenomic-based免疫的问题,而不是一个失败的部分遵循说明基本卫生或使用足够的酸果蔓汁。
更多信息:Seongmi k . Russell et al, Uropathogenic大肠杆菌侵染诱导上皮训练免疫影响泌尿道疾病的结果,微生物学性质(2023)。DOI: 10.1038 / s41564 - 023 - 01346 - 6
Soumitra莫汉蒂、约翰·克尔白和Annelie布劳恩,表观遗传修饰的影响尿路感染的结果,微生物学性质(2023)。DOI: 10.1038 / s41564 - 023 - 01371 - 5
©2023科学欧宝app网彩X网络