新技术开启了大门到安全的基因编辑通过减少突变基因治疗的问题

CRISPR-Cas9被广泛用于编辑感兴趣的基因组研究基因和修改疾病有关的基因。然而,这一过程与副作用包括不必要的突变和毒性。因此,一个新技术,减少这些副作用需要改善其有用性在工业和医学。
现在,研究人员在日本南部九州大学和名古屋大学医学院在日本中部已经开发出一种优化基因编辑方法,大大降低了突变,打开大门遗传疾病的更有效的治疗。他们的发现发表在自然生物医学工程。
基因编辑科技革命,是以CRISPR-Cas9食物和医疗行业。在技术、Cas9核酸酶,这种酶削减DNA,引入细胞合成RNA (gRNA)指南,指导酶到所需的位置。通过削减基因组,多余的基因可以删除,新的(功能)的基因可以在轻松快速地补充道。
基因组编辑的缺点之一是,人们越来越担心突变和脱靶效应。这通常是由于酶的目标基因的网站有一个序列类似于目标站点。同样,在染色体水平可能发生突变基因改变时,这阻碍了基因治疗癌症的临床试验,甚至导致死亡的患者接受治疗肌肉萎缩症。集团假设当前编辑协议使用Cas9造成过度DNA乳沟,导致一些突变。
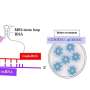
来测试这一假说,一群组成的助理教授正树川俣町九州大学和名古屋大学研究生院Hiroshi Suzuki教授医学构造一个系统称为“目标”老鼠细胞,评估活动的Cas9分别为每个染色体。他们的研究结果表明,常用的方法是与很高的编辑活动有关。他们决定这高活动造成的一些不必要的副作用,所以他们寻找gRNA改性方法可以抑制它。他们发现一个额外的胞嘧啶扩展的5 '端gRNA是有效的“保护”过度活跃和允许控制DNA乳沟。他们称这种微调系统维护gRNA ([C] gRNA)。
他们的结果是惊人的。利用他们的新技术,非目标效应和细胞毒性降低,single-allele选择性编辑的效率增加,homology-directed修复的效率,最常使用的DNA双链断裂修复的机制,是加强。
测试其有效性在医疗环境中,他们调查了罕见的疾病叫fibrodysplasia ossificans progressiva。使用一个小鼠模型,他们能够创造出同样的基因型为人类的疾病。然后利用iPS细胞,他们能够精确修复损伤到变异等位基因的单核苷酸特别引起疾病,展示他们的技术的实用性作为安全有效的基因治疗方法。
该小组还建造第一个各种基因编辑模式之间的相关性的数学模型和Cas9活动,这将使基因组编辑的用户模拟结果在整个细胞群。这一突破性的将允许研究人员确定Cas9活动最大化效率,减少所需的巨大的成本和劳动力。
“我们建立了一个新的基因组编辑平台,可以通过开发所需的编辑效率最大化activity-regulating [C] gRNAs适当Cas9活动。此外,我们发现,“维护gRNA”可以应用于各种CRISPR工具要求gRNAs通过调节他们的活动,比如使用Cas12a,不同的DNA裂解机制,”铃木教授说。
”技术,使用Cas9激活或抑制基因的利益,如CRISPR激活和CRISPR干扰,过度诱导或抑制基因表达可能不是有用的,甚至有害细胞。控制表达水平[C] gRNA是一项重要的技术,可用于各种应用,包括精确的基因疗法的实施。”
集团目前正在启动商业计划传播新的基因组编辑平台。“特别是,我们相信,这项技术可以使医学领域的重大贡献,“川俣町博士说。“我们正在评估其治疗效果和选定目标疾病在细胞和安全动物实验和使用它来帮助开发治疗药物和基因治疗方法,特别是对于罕见疾病的治疗方法还没有被建立。”
更多信息:正树川俣町,优化Cas9活动single-guide rna,通过增加胞嘧啶的扩展自然生物医学工程(2023)。DOI: 10.1038 / s41551 - 023 - 01011 - 7。www.nature.com/articles/s41551 - 023 - 01011 - 7