定制T细胞免疫疗法使用新的“SNAPtag”技术
匹兹堡大学的研究人员已经开发出一种普遍的受体系统,允许T细胞识别任何细胞表面目标,使高度可定制的汽车T细胞和其他免疫疗法治疗癌症和其他疾病。发现可以延伸到实体肿瘤,使更多的病人获得汽车T细胞疗法产生了改变游戏规则的结果在某些血液癌症。
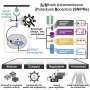
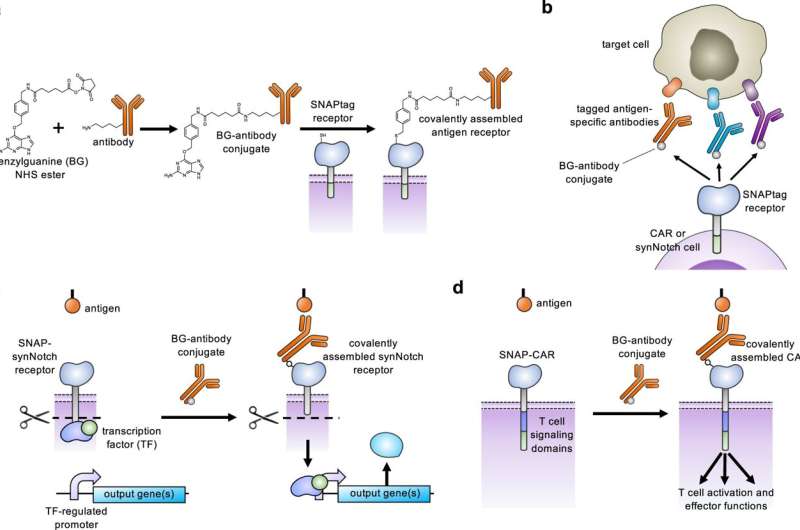
描述在一个自然通讯今天发表的研究,5月9日,新方法包括工程T细胞受体轴承通用“SNAPtag”融合抗体针对不同的蛋白质。通过调整这些抗体的类型或剂量,治疗可以为最佳的免疫反应。
研究人员表明,他们的快速方法在两个重要的受体:汽车受体合成T细胞受体坐标一系列免疫反应,和SynNotch,合成受体可以被编程来激活任何基因。的,定制的疗法的可能性几乎是无穷无尽的。
“我们首次显示,我们可以做一个通用SynNotch受体。这个SNAP-SynNotch系统是超可编程,因为你可以同时拥有设计师输入和输出设计师基因,”杰森Lohmueller资深作者博士说,手术和免疫学助理教授肿瘤外科分部的皮特医学院和研究员UPMC希尔曼癌症中心。“我们的希望是,我们可以用这种方法使细胞治疗和癌症基因,自身免疫性疾病、器官移植宽容等等。”
汽车T细胞免疫疗法涉及工程患者自身的细胞,T细胞受体识别一个特定的蛋白在肿瘤细胞注射回患者。
与汽车T疗法”的一个重大问题是,您的目标只有一个蛋白质,“Lohmueller解释道。“如果肿瘤发展失去蛋白质或表达下调,你需要重新设计T细胞,这是一个高度相关的和昂贵的过程。”
Lohmueller解决这个问题,第一作者Elisa Ruffo,博士,博士后研究员皮特,亚历山大•Deiters博士,皮特的化学教授及其同事开发普遍SNAP-CAR T细胞通过添加SNAPtag酶受体。这些细胞管理随着肿瘤靶向抗体,称为benzylguanine用分子标记。
通过bio-orthogonal chemistry-a类型的反应发生在不干扰自然生命系统处理与benzylguanine SNAPtag反应,融合受体的抗体。同时添加不同的抗体,或一个接一个,允许受体识别不同的肿瘤特征。
“我们的方法有什么独特的T细胞与抗体的相互作用。不仅仅是约束力,但通过共价化学键的attachment-the最强的形式,融合“Lohmueller解释道。“这种bio-orthogonal方法已被证明在动物成像的目的,但是我们最早用它治疗,所以我们真的共价的突破技术。”
这紧张的债券的优势意味着受体的激活可以实现较低剂量的抗体,Lohmueller说。使用数学建模,亚当Butchy和娜塔莎Miskov-Zivanov研究生,博士,助理的电气和计算机工程教授皮特Swanson工程学院的,表明它可能也有可能从较弱的抗体和之间的交互活动肿瘤细胞类型的癌症提供更大的灵活性,可以有针对性的蛋白质。
共价键也创建SNAP-SynNotch细胞的秘密配方。SynNotch受体被激活时,机械牵引力量伸展的受体暴露部分蛋白质,然后将发布一个转录因子,旅行细胞核选择基因的表达。
“我们发现,我们需要共价键的强度来承受拉力,“Lohmueller解释道。“如果我们只受体抗体之间的绑定,将受体破裂,我们不会得到信号。”
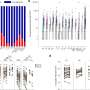
研究人员表明,他们普遍SNAP-CAR和SNAP-SynNotch受体可以被激活,以应对不同的目标通过添加相应的抗体。SNAP-CAR T细胞还可以同时多个目标蛋白质在不同类型的细胞,这表明他们可能有助于避免导致的癌症复发肿瘤的变化目标或损失的目标。
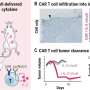
小鼠模型的癌症,治疗SNAP-CAR T细胞萎缩肿瘤和大大延长生存,一个重要的概念验证,测试这种方法奠定了基础临床试验与Coeptis疗法,从皮特SNAP-CAR技术许可。
更多信息:Elisa Ruffo et al,翻译后共价组装的汽车和可编程的抗原定位synNotch受体,自然通讯(2023)。DOI: 10.1038 / s41467 - 023 - 37863 - 5。www.nature.com/articles/s41467 - 023 - 37863 - 5