研究人员发现癌症劫持一个类燃料肿瘤发生的突变酶图案
癌症蔓延在整个人体的狡猾,几乎军国主义方式。例如,它可以操纵我们的基因组成,占领特定的细胞间信号流程,促进肿瘤的生长和变异的关键酶,抗拒治疗,并加速其从原始网站传播血液或其他器官。
酶突变已经引起了科学家们的极大兴趣,研究癌症。刘和谭实验室的科学家在UNC Lineberger综合癌症中心一直在研究突变酶识别的图案在基质中,这可能更忠实地反映酶的功能有可能找到新的目标或方向癌症治疗。
“我们认为理解角色的突变酶底物,酶作为一个整体,而是可能有助于提高靶向治疗的疗效,尤其是对酶都有致癌和肿瘤抑制功能通过控制不同的基质的子集,“剑锋Chen说博士,谁是第一作者,在刘实验室博士后UNC部门的生物化学和生物物理学。
他们的研究结果发表在实验医学杂志2023年6月29日。
AGC突变激酶图案
使用开发算法和信息从癌症基因组图谱(TCGA),研究人员发现,最高的突变发生在AGC激酶主题叫做RxRxxS / T。RxRxxS / T是一个短,重复出现的模式,AGC的~ 60激酶家族之间共享。这些酶中扮演关键的角色转移,扩散、耐药性和发展。
“我们发现癌症试图逃避或创建突变在这些RxRxxS / T图案,给自己更多的优势肿瘤的生长和生存,”均说刘博士,生物化学和生物物理学副教授。
结直肠癌的新机制
刘和棕褐色组织进行了验证研究AGC激酶与结直肠癌相关主题的突变,第二最致命的癌症和第三世界中最常见的恶性肿瘤。目前,结肠直肠癌的5年生存率为12%。
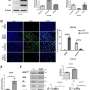
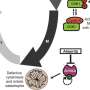
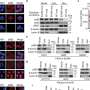
他们发现,结肠癌“劫持”BUD13突变,蛋白质编码基因,回避由AGC激酶的磷酸化。结肠癌最终喜欢这些BUD13突变,因为它获得一个额外的好处的灭活一个叫做Fbw7 E3连接酶。Fbw7“关闭”,一个至关重要的肿瘤抑制,使肿瘤生长和治疗耐药性的增加。
除了他们的发现在Fbw7失活,该研究小组还发现,BUD13肿瘤细胞更容易受到mTORC2激酶的抑制,揭示一个新的、潜在的靶向治疗结肠癌病人的轴承BUD13突变。
“这是令人兴奋的,梳理不同类型的体细胞突变,我们很高兴提供癌症研究社区公开可用的资源,“鲜明Tan说,博士,谁是生物统计学的研究助理教授在针梳公共卫生学院和Lineberger综合癌症中心。
搜索蛋白质主题TCGA的突变数据库,点击在这里。
更多信息:剑锋陈et al,躯体功能的突变BUD13促进肿瘤形成通过扰乱Fbw7函数,实验医学杂志(2023)。DOI: 10.1084 / jem.20222056